��Ŀ����
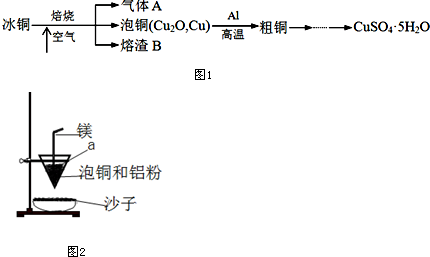
6����������������ƶ��dz�����ʳƷ������I����������Ʊ�����Ϊͼ1��
�����������£�
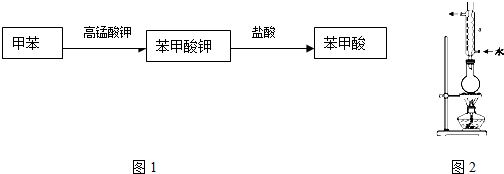
����Բ����ƿ�м���һ�����ļױ���������ˮ����װ����ͼ ��ʾ��Ӧװ�ã��������У�
�ڴ�a���Ͽڷ����μ���һ�����ļ��Ը�����أ���������ˮ��ϴa���ڱڣ�����������ʱ��ҡ����ƿ��ֱ����Ӧ����������
�۽���Ӧ���Һ���ȹ��ˣ�����Ϊ��ɫ���壻�õ�����Һ�������ɫ���ɼ��������ı�������������Һʹ��ɫ��ȥ�����¹��ˣ��ٽ���Һ���ڱ�ˮԡ����ȴ����Ũ�����ữ��ֱ����Ʒ������
��1������a�����������ܣ�����������Ҫ�����Ǽױ�
��2��д���μӱ�������������Һʱ�����ӷ���ʽ2MnO4-+H2O+3SO32-�T2 MnO2��+2OH-+3SO42-
��3���ڢ۲��У�����ȴ���ٹ��ˣ������ƫ�ͣ��ƫ�ߡ��������䡱��ƫ�͡���
���������Ƶζ����������������Ƶζ�Һ��������Һ���뷼��������������ص�����Ӧͼ2�����������ص��Σ����ⶨҩ�ﺬ���ķ�������ζ���Ӧ���£�
Ar-NH2+NaNO2+2HCl��Ar-N2C1+NaCl+2H2O
��4����֪��������������ԣ�ʵ������KI-������Һ��Ϊ�ζ��յ��ָʾ������ζ��յ��������Һ����ɫ����ɫ�����ڰ�����ڲ���ɫ��
��5�����й�ҩ�䡷�涨�����£�10��-30�棩�����¿��ٵζ����¶�̫��ʹ������ӷ��ͷֽ⣬�ⶨ�����ƫ�ߣ����ƫ�ߡ���ƫ�͡�����Ӱ�족�������¶�Ҳ���˹��ͣ�ԭ���Ƿ�Ӧ���ʹ����������ڵζ��յ���жϣ�
���� I����������Ʊ����������ϵ������ɱ����Ը�������������Ȼ����ױ���������������ɱ�����أ��������ữ���ɱ����ᣮ
��1�����ݳ������������ƺ���;��𣻼ױ��е�ͣ�����������Ҫ�����Ǽױ���
��2��KMnO4��Һ�������ԣ�������������Һ�л�ԭ�ԣ����ᷢ��������ԭ��Ӧ��������������Ԫ�ؿ��Ա���������������ڼ��������¸�����صĻ�ԭ����MnO2�����ݻ��ϼ�����������Ƚ������ӷ���ʽ��д��
��3�����ڸ����ʵ��ܽ�����¶ȵ����߶�����������ܽ���ڽϸߵ��¶��±Ƚϴ�����ȴ���ٹ��ˣ��־�����������ƫ�ͣ�
��4���ⵥ������������ɫ�������������Ե��������뷼��������������ص�����Ӧ��ɣ��ٵζ������������������ӣ��ⵥ�ʺ͵���������ɫ���֣����ڰ�����ڲ���ɫ��
��5���¶�̫��ʹ������ӷ��ͷֽ⣬������뷼��������������ص�����Ӧ���ⶨ�����ƫ�ߣ��¶ȹ��ͣ���Ӧ���ʹ����������ڵζ��յ���жϣ�
��� �⣺I����������Ʊ����������ϵ������ɱ����Ը�������������Ȼ����ױ���������������ɱ�����أ��������ữ���ɱ����ᣮ
��1������a���������ױ���Ϊ�����ܣ��ڳ����¼ױ���Һ�壬�������ǹ��壬�ڢٲ��мױ��е�ϵͣ�����ʱ�ӷ������ڵڢٲ�����Ҫ�ǶԼױ����л�����
�ʴ�Ϊ�������ܣ��ױ���
��2��KMnO4��Һ�������ԣ�������������Һ�л�ԭ�ԣ����ᷢ��������ԭ��Ӧ�����Ը�����أ���ԭ����ΪMnO2�����ݻ��ϼ�����������ȣ�S��+4��+6����2����3��Mn��+7��+4����3����2����SO32-��SO42-�Ļ�ѧ������Ϊ3��MnO4-��MnO2�Ļ�ѧ������Ϊ2����O�غ��֪��H2O�Ļ�ѧ������Ϊ1�����Եμӱ�������������Һʱ�����ӷ���ʽΪ��2MnO4-+H2O+3SO32-�T2MnO2��+2OH-+3SO42-��
�ʴ�Ϊ��2MnO4-+H2O+3SO32-�T2MnO2��+2OH-+3SO42-��
��3��������еõ����DZ�����أ����ữ���Եõ������ᣬ���ڸ����ʵ��ܽ�����¶ȵ����߶�����������ܽ���ڽϸߵ��¶��±Ƚϴ�Ӧ�ڽϸߵ��¶���ʹ�������γɱ�����Һ���۽���Ӧ���Һ���ȹ��ˣ�Ȼ������ȴ�ᾧ�γɹ��壬�����˵õ������ᾧ�壬����ȴ���ٹ��ˣ��־�����������̽��������������ƫ�ͣ�
�ʴ�Ϊ��ƫ�ͣ�
��4����KI-������Һ��Ϊ�ζ��յ��ָʾ�����������Ƶζ�Һ��������Һ���뷼��������������ص�����Ӧ������Ӧ��ɣ����������Ե��������������������ɵⵥ�ʣ��������ʾ��ɫ�����Եζ��յ�����Ϊ����Һ����ɫ����ɫ�����ڰ�����ڲ���ɫ��
�ʴ�Ϊ����Һ����ɫ����ɫ�����ڰ�����ڲ���ɫ��
��5���������ӷ����ֽ�2HNO2$\frac{\underline{\;\;��\;\;}}{\;}$H2O+NO2��+NO�����¶�̫��ʹ������ӷ��ͷֽ⣬������뷼��������������ص�����Ӧ���ⶨ�����ƫ�ߣ��¶ȹ��ͣ���Ӧ���ʹ����������ڵζ��յ���жϣ�
�ʴ�Ϊ��ƫ�ߣ���Ӧ���ʹ����������ڵζ��յ���жϣ�
���� ���⿼����������ԭ��Ӧԭ������ѧʵ�������Ļ���ʹ�ã����ʵķ��벽�衢��ȡ������������ѡ���Ƕ�֪ʶ���ۺ����������������������Ŀ��飬���ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�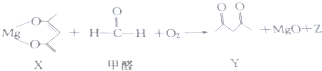
�����йظ÷�Ӧ��˵����ȷ���ǣ�������
| A�� | Z�ĽṹʽΪO-C-O | B�� | X�ǻ�ԭ�� | ||
| C�� | ��ȩ�������� | D�� | ��ȥ1mol��ȩʱ��ת��4mol���� |
| A�� | ������ B ��ʾ�ķ�Ӧ��ƽ������Ϊ 0.6 mol•L-1•s-1 | |
| B�� | 2 s ʱ���� B ��Ũ��Ϊ 0.7 mol•L-1 | |
| C�� | 2 s ʱ���� A ��ת����Ϊ70% | |
| D�� | ������ A ��ʾ�ķ�Ӧ��ƽ������Ϊ 0.3 mol•L-1•s-1 |
��1����֪��H-H����Ϊ436KJ•mol-1��N��N����Ϊ945KJ•mol-1��N-H����Ϊ391KJ•mol-1��д���ϳɰ���Ӧ���Ȼ�ѧ����ʽ��N2��g��+3H2��g��?2NH3��g����H=-93 KJ•mol-1
��2�����淴ӦN2+3H2?2NH3�ں����ܱ������н��У��ﵽƽ��״̬�ı�־�Ǣڢ�
�ٵ�λʱ��������n mo1N2��ͬʱ����3n mol H2
�ڵ�λʱ����1��N��N�����ѵ�ͬʱ����6��N-H������
��������N2��H2��NH3�����ʵ���Ϊ1��3��2
�ܳ����£����������ܶȲ��ٸı��״̬
�ݳ����£���������ƽ����Է����������ٸı��״̬
��3�������£���һ��2L���ܱ������г���2.6mol H2��1mol N2����Ӧ�����ж�NH3��Ũ�Ƚ��м�⣬�õ����������±�����
| ʱ��/min | 5 | 10 | 15 | 20 | 25 | 30 |
| C��NH3��/mol•L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
��4�����ǵ��ʹ�ҵ����Ҫԭ�ϣ�ij���ʳ�����Ȼʯ�����Ҫ�ɷ�CaSO4��Ϊԭ�������̬���ʣ�NH4��2SO4������֪Ksp��CaSO4��=7.10��10-5 Ksp��CaCO3��=4.96��10-9���乤���������£�

��д���Ʊ���NH4��2SO4�ķ�Ӧ����ʽ��CaSO4+��NH4��2CO3=��NH4��2SO4+CaCO3�����������й����ݼ���������Ӧ�ܷ�����ԭ����ΪKsp��CaSO4��=7.10��10-5��Ksp��CaCO3��=4.96��10-9��

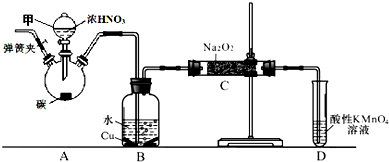
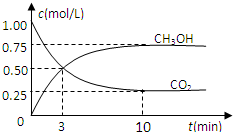 �������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӣ�Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬�����Ϊ1L���ܱ������У�������䣩������1mol CO2��3mol H2��һ�������·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49.0kJ/mol�����CO2��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ��
�������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӣ�Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬�����Ϊ1L���ܱ������У�������䣩������1mol CO2��3mol H2��һ�������·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49.0kJ/mol�����CO2��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ��