题目内容
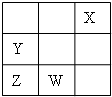 W、X、Y、Z为短周期元素,在周期表中位置如图所示,有关元素W、X、Y、Z的叙述,不正确的是( )
W、X、Y、Z为短周期元素,在周期表中位置如图所示,有关元素W、X、Y、Z的叙述,不正确的是( )| A、通常情况下四种元素的单质中,X化学性质最稳定 |
| B、四种元素都能与氢元素形成稳定的化合物 |
| C、Y、Z离子最外层电子数相同 |
| D、四种元素中Z元素最高价氧化物对应的水化物酸性最强 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:W、X、Y、Z为短周期元素,由元素在周期表中位置,可知W为He、Y为O、Z为S、W为Cl,结合元素周期律与元素化合物性质解答.
解答:
解:W、X、Y、Z为短周期元素,由元素在周期表中位置,可知W为He、Y为O、Z为S、W为Cl,
A.四种单质中X为稀有气体,化学性质最稳定,故A正确;
B.He不能与氢气形成化合物,故B错误;
C.氧离子、硫离子最外层电子数都是8,故C正确;
D.四种元素中Cl氯气非金属性最强,其最高价氧化物对应水化物的酸性最强,故D错误,
故选BD.
A.四种单质中X为稀有气体,化学性质最稳定,故A正确;
B.He不能与氢气形成化合物,故B错误;
C.氧离子、硫离子最外层电子数都是8,故C正确;
D.四种元素中Cl氯气非金属性最强,其最高价氧化物对应水化物的酸性最强,故D错误,
故选BD.
点评:本题考查元素周期表与元素周期律应用,难度不大,侧重对基础知识的巩固,注意整体把握元素周期表结构.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
第3周期元素的基态原子中,不可能出现d电子,主要依据是( )
| A、能量守恒原理 | B、泡利原理 |
| C、洪特规则 | D、构造原理 |
下列有关电解质溶液的说法正确的是( )
| A、将pH=2的NH4Cl与pH=12氨水等体积混合,溶液中:c(NH4+)=c(Cl-) | ||||
| B、溶液中c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) | ||||
| C、1.0mol?L-1的H2SO4溶液80℃时的pH大于25℃时pH | ||||
D、对氨水进行稀释,
|
某学生提供的实验数据如下,其中肯定错误的是( )
①用10mL的量筒量取5.60mL的液体
②用托盘天平称取22.5g KCl
③酸碱中和滴定时,消耗0.1000mol/L的盐酸23.25mL
④用广泛pH试纸测得某溶液的pH=4.4.
①用10mL的量筒量取5.60mL的液体
②用托盘天平称取22.5g KCl
③酸碱中和滴定时,消耗0.1000mol/L的盐酸23.25mL
④用广泛pH试纸测得某溶液的pH=4.4.
| A、①② | B、②③ | C、③④ | D、①④ |
甲基环己烷可由甲苯与氢气加成制得,其环上一氯代物的同分异构体数目是( )
| A、4 | B、3 | C、2 | D、1 |
1g氢气燃烧生成液态水放出142.9kJ的热量,表示该反应的热化学方程式正确的是( )
| A、2H2(g)+O2(g)═2H2O(l)△H=-142.9 kJ?mol-1 | ||
B、H2(g)+
| ||
| C、2H2+O2═2H2O△H=571.6 kJ?mol-1 | ||
D、H2(g)+
|
元素X、Y可组成化学式为XY2的离子化合物,则X、Y的原子序数可能是( )
| A、11和16 | B、6和8 |
| C、13和17 | D、20和9 |