题目内容
1g氢气燃烧生成液态水放出142.9kJ的热量,表示该反应的热化学方程式正确的是( )
| A、2H2(g)+O2(g)═2H2O(l)△H=-142.9 kJ?mol-1 | ||
B、H2(g)+
| ||
| C、2H2+O2═2H2O△H=571.6 kJ?mol-1 | ||
D、H2(g)+
|
考点:热化学方程式
专题:化学反应中的能量变化
分析:根据物质的物质的量与反应热成正比,计算1mol氢气燃烧生成液态水放热,结合热化学方程式的书写要求,标注物质聚集状态和对应反应的焓变得到.
解答:
解:A、1g氢气燃烧生成液态水,放出142.9kJ热量,所以2mol氢气燃烧生成液态水,放出的热量为142.9kJ×4=571.6kJ,所以△H=-571.6kJ?mol-1,故A错误;
B、1gH2燃烧生成液态水时放出142.9kJ的热量,△H<0,热化学方程式为H2(g)+
O2(g)=H2O(l)△H=-285.8kJ?mol-1,故B正确.
C、物质的状态影响反应热,未注明物质的聚集状态,故C错误;
D、依据题干是1g氢气燃烧生成液态水,而热化学方程式中是生成气态水,故D错误;
故选B.
B、1gH2燃烧生成液态水时放出142.9kJ的热量,△H<0,热化学方程式为H2(g)+
| 1 |
| 2 |
C、物质的状态影响反应热,未注明物质的聚集状态,故C错误;
D、依据题干是1g氢气燃烧生成液态水,而热化学方程式中是生成气态水,故D错误;
故选B.
点评:本题考查了热化学方程式的书写方法和注意问题,注意反应热化学方程式需要标注物质聚集状态,对应量的反应热,题目较简单.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
以下微粒含配位键的是( )
①N2H5+;②CH4;③OH-;④NH4+;⑤Fe(CO)3;⑥Fe(SCN)3;⑦H3O+;⑧Ag(NH3)2OH.
①N2H5+;②CH4;③OH-;④NH4+;⑤Fe(CO)3;⑥Fe(SCN)3;⑦H3O+;⑧Ag(NH3)2OH.
| A、①②④⑦⑧ | B、③④⑤⑥⑦ |
| C、①④⑤⑥⑦⑧ | D、全部 |
下列表示正确的是( )
| A、含有大量AlO2-的溶液中:K+、Al3+、Br-、HCO3-可共存 |
| B、CO(g)的燃烧热是283.0kJ?mol-1,则2CO2(g)═2CO(g)+O2(g)反应的△H=+566.0kJ?mol-1 |
| C、将SO2通入Ca(ClO)2溶液中:Ca2++2ClO-+SO2+H2O═CaSO3+2HClO |
| D、在某钠盐溶液中含有等物质的量的Cl-、I-、SO32-、CO32-、NO3-、SiO32-中一种或多种,当加入过量的盐酸产生气泡,溶液颜色变深但仍澄清,阴离子种数减少3种,则原溶液中一定有CO32- |
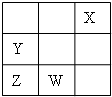 W、X、Y、Z为短周期元素,在周期表中位置如图所示,有关元素W、X、Y、Z的叙述,不正确的是( )
W、X、Y、Z为短周期元素,在周期表中位置如图所示,有关元素W、X、Y、Z的叙述,不正确的是( )| A、通常情况下四种元素的单质中,X化学性质最稳定 |
| B、四种元素都能与氢元素形成稳定的化合物 |
| C、Y、Z离子最外层电子数相同 |
| D、四种元素中Z元素最高价氧化物对应的水化物酸性最强 |
下列说法中正确的是( )
| A、全部由极性键构成的分子一定是极性分子 |
| B、非极性分子中一定没有极性键 |
| C、离子化合物中一定没有共价键 |
| D、共价化合物中一定没有离子键 |
化学与科学、技术、社会、环境密切相关.下列叙述正确的是:①NO2、CO2和SO2都是大气污染物;②为了防止食品受潮变质,常在食品包装袋中放入活性铁粉;③单质硅是将太阳能转变为电能的常用材料;④维生素C易失电子,在人体内起抗氧化作用( )
| A、①② | B、②③ | C、③④ | D、①④ |
苯环结构中不存在C-C单键与C=C双键的交替结构,可以作为证据的是( )
①苯不能使溴水反应褪色
②苯不能使酸性高锰酸钾溶液褪色
③苯在一定条件下既能发生取代反应,又能发生加成反应
④经测定,邻二甲苯只有一种结构
⑤苯是正六边形.
①苯不能使溴水反应褪色
②苯不能使酸性高锰酸钾溶液褪色
③苯在一定条件下既能发生取代反应,又能发生加成反应
④经测定,邻二甲苯只有一种结构
⑤苯是正六边形.
| A、①②④⑤ | B、①③④⑤ |
| C、①②③④ | D、②③④⑤ |
有等体积的NaCl、CaCl2、AlCl3溶液,完全沉淀其中的Cl-消耗同浓度的AgNO3溶液体积相等,则三种溶质的浓度之比为( )
| A、1:1:1 |
| B、1:2:3 |
| C、6:3:2 |
| D、3:2:1 |