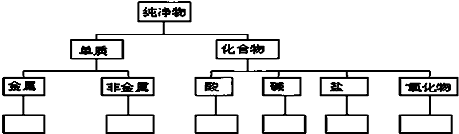
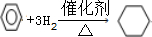
题目内容
4.以下物质间的每步转化通过一步反应能实现的是( )| A. | Al→Al2O3→Al(OH)3→NaAlO2 | B. | Si→SiO2→H2SiO3→Na2SiO3 | ||
| C. | N2→NO→NO2→HNO3 | D. | S→SO3→H2SO4→MgSO4 |
分析 A.Al2O3应先与酸反应生成Al3+,然后与碱反应生成Al(OH)3,不能一步实现;
B.SiO2不能用水反应生成H2SiO3;
C.可通过N2$\stackrel{O_{2}}{→}$NO$\stackrel{O_{2}}{→}$NO2→HNO3等反应实现;
D.S不能直接生成SO3.
解答 解:A.Al2O3应先与酸反应生成Al3+,然后与碱反应生成Al(OH)3,不能一步实现,故A错误;
B.SiO2不能用水反应生成H2SiO3,应先和NaOH反应生成Na2SiO3,然后和酸反应生成H2SiO3,不能一步实现,故B错误;
C.可通过N2$\stackrel{O_{2}}{→}$NO$\stackrel{O_{2}}{→}$NO2→HNO3等反应实现,每步转化通过一步反应能实现,故C正确;
D.S不能直接生成SO3,S氧气在点燃的条件下反应生成SO2,SO2与氧气在催化剂的条件下可生成SO3,不能一步实现,故D错误;
故选C.
点评 本题考查元素化合物知识,题目难度中等,学习中牢固掌握相关基础知识,此类题目可轻松解答.

练习册系列答案
相关题目
15.某学生为了探究锌与盐酸反应生成氢气过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
(1)哪一时间段反应速率最大2~3min,原因是反应放热,加快反应速率.(指0~1、1~2、2~3、3~4、4~5min)
(2)哪一段时段的反应速率最小4~5min,原因是盐酸浓度减小(氢离子浓度减小)(.
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,可在盐酸中分别加入等体积的下列溶液,你认为可行的是B.
A.Na2CO3溶液 B.NaCl溶液 C.NaNO3溶液 D.CuSO4溶液
(4)如果要使产生氢气的速率加快你认为可行的措施有哪些?(至少写两条)升温、增大盐酸浓度(或加入少量的硫酸铜溶液;减小锌粉的颗粒度).
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(2)哪一段时段的反应速率最小4~5min,原因是盐酸浓度减小(氢离子浓度减小)(.
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,可在盐酸中分别加入等体积的下列溶液,你认为可行的是B.
A.Na2CO3溶液 B.NaCl溶液 C.NaNO3溶液 D.CuSO4溶液
(4)如果要使产生氢气的速率加快你认为可行的措施有哪些?(至少写两条)升温、增大盐酸浓度(或加入少量的硫酸铜溶液;减小锌粉的颗粒度).
12.下列物质的电子式书写正确的是( )
| A. | CH3OH 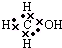 | B. | HClO 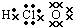 | C. | N2 | D. | OH- |
19.通过复习总结,下列归纳正确的是( )
| A. | 有单质参加的反应,置换反应一定都属于氧化还原反应 | |
| B. | 简单非金属阴离子只有还原性,而金属阳离子只有氧化性 | |
| C. | 离子化合物在熔融态都能够导电,共价化合物在熔融态都不导电 | |
| D. | 所有物质都有化学键 |
13.冰融化为水的过程的焓变和熵变正确的是( )
| A. | △H>0,△S<0 | B. | △H<0,△S>0 | C. | △H>0,△S>0 | D. | △H<0,△S<0 |
14.下列说法正确的是( )
| A. | 丙烯分子中有7个σ键,2个π键 | |
| B. | 在60 g SiO2晶体中,Si-O键的数目为2NA | |
| C. | 共价键有方向性,但无饱和性 | |
| D. | 由ⅠA族和ⅥA族元素形成的原子个数比为1:1、电子总数为38的化合物,是含有共价键的离子化合物 |