题目内容
8.某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5um的悬浮颗粒物)其主要来源为燃煤、机动车尾气等. 因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:(1)对PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:离子 K+ Na+ NH4+ SO42- NO3- Cl-
浓度/mol•L-1 4×10-6 6×10-6 2×10-5 4×10-5 3×10-5 2×10-5
根据表中数据判断PM2.5的酸碱性为酸性,试样的pH值=4.
(2)为减少SO2的排放,常采取的措施有:
将煤转化为清洁气体燃料.已知:
H2(g)+1/2O2(g)=H2O(g)△H=-241.8kJ/mol
C(s)+1/2O2(g)=CO(g)△H=-110.5kJ/mol
写出焦炭与水蒸气反应的热化学方程式C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ/mol;
(3)汽车尾气中NOx和CO的生成及转化
①已知气缸中生成NO的反应为:
N2(g)+O2(g)?2NO(g)△H>0
若1mol空气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡.测得NO为8×10-4mol.计算该温度下的平衡常数约为K=4×10-6.
汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是温度升高,反应速率加快,平衡右移.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g)已知该反应的△H>0,简述该设想能否现的依据:该反应是焓增、熵减的反应.根据△G=△H-T△S,△G>0,不能实现.
③目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$ 2CO2+N2.
分析 (1)观察表格中发现NH4+水解显酸性,PM2.5的酸碱性为酸性;
(2)利用盖斯定律计算反应热,将②-①可得;
(3)①计算出平衡时各种物质的物质的量,结合平衡常数的表达式计算,依据化学反应速率和平衡移动原理分析判断;
②根据G=△H-T•△S判断反应能否自发进行;
③CO和NO催化氧化生成氮气和二氧化碳;
解答 解:(1)观察表格中发现NH4+水解显酸性,PM2.5的酸碱性为酸性.试样的pH值根据溶液中电荷守恒计算H+离子浓度为10-4,PH值为4,故答案为:酸性;4;
(2)①已知:①H2 (g)+$\frac{1}{2}$O2 (g)=H2O(g);△H=-241.81kJ•mol-1,
②C (s)+$\frac{1}{3}$O2 (g)=CO (g);△H=-110.51kJ•mol-1,
利用盖斯定律,将②-①可得C(s)+H2O(g)=CO(g)+H2(g);△H=(-110.51kJ•mol-1)-(-241.81kJ•mol-1)=++13l.3 kJ•mol-1;
故答案为:C(s)+H2O(g)=CO(g)+H2(g);△H=+13l.3 kJ•mol-1;
(3)①已知气缸中生成NO的反应为:N2(g)+O2(g)?2NO(g)△H>0.若气缸中进入1mol空气(1mol空气含有0.8mol N2和0.2mol O2),1300℃时在密闭容器内反应达到平衡.测得NO为8×10-4mol,反应前后气体物质的量相同,计算平衡常数时可以用物质的量代替平衡浓度计算,先计算物质的平衡量,N2为0.8mol-4×10-4 mol,O2为0.2mol-4×10-4 mol,带入平衡常数表达式即可,书写计算得K=$\frac{{c}^{2}(NO)}{c({N}_{2})c({O}_{2})}$=$\frac{(8×1{0}^{-4}mol)^{2}}{(0.8-4×1{0}^{-4})mol×(0.2-4×1{0}^{-4})mol}$=4×10-6,气缸温度越高,单位时间内NO排放量越大,原因是温度升高,反应速率加快,平衡右移;
故答案为:4×10-6;温度升高,反应速率加快,平衡右移;
②2CO(g)=2C(s)+O2(g),该反应是焓增、熵减的反应.根据G=△H-T•△S,G>0,不能实现;
故答案为:该反应是焓增、熵减的反应.根据△G=△H-T△S,△G>0,不能实现;
③CO和NO催化氧化生成氮气和二氧化碳,反应的化学方程式为:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2,
故答案为:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2;
点评 本题综合考查化学反应原理的基础知识,涉及离子的水解、PH值的计算、盖斯定律的应用、化学平衡常数的计算、自由能的应用等,题目难度中等,注意相关知识的积累.

| A. | 前2 s,以N2O4的浓度表示的平均反应速率为 0.01 mol•L-1•s-1 | |
| B. | 在2 s时体系内的压强为开始时的1.1倍 | |
| C. | 在平衡时体系内含N2O40.25 mol | |
| D. | 平衡时,如果压缩容器容积,则可提高N2O4的转化率 |
( )
| A. | (3)(7)(9)(10)(11)(12) | B. | (3)(7)(9)(10)(11)(14) | C. | (3)(7)(8)(9)(10)(11)(12) | D. | (1)(3)(7)(8)(9)(10)(11)(12) |
| A. | Mg2+、NH4+、SO42-、Cl- | B. | Cu2+、Na+、HCO3-、OH- | ||
| C. | K+、Ca2+、NO3-、CO32- | D. | Ag+、Fe3+、Cl-、NO3- |
 某混合溶液中,一定含有Cl-、Br-、I-,可能含有的离子如下表所示.
某混合溶液中,一定含有Cl-、Br-、I-,可能含有的离子如下表所示.| 可能大量含有的阳离子 | H+、Ag+、Mg2+、Al3+、NH4+、Fe3+ |
| 可能大量含有的阴离子 | CO32-、AlO2-、NO3- |
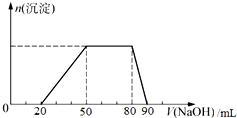
探究一:取10mL该混合溶液,向其中逐滴加入氢氧化钠溶液,产生沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)的关系如图所示.
探究二:取1L该混合溶液,向该溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如下表所示.
| Cl2的体积(标准状况) | 5.6L | 11.2L | 22.4L |
| n(Cl-) | 2.5mol | 3.0mol | 4.0mol |
| n(Br-) | 3.0mol | 2.8mol | 1.8mol |
| n(I-) | X mol | 0 | 0 |
| A. | X=0.3 | |
| B. | 溶液中n(Cl-):n(Br-):n(I-)=10:15:4 | |
| C. | 加入的氢氧化钠溶液的浓度为1.45mol•L-1 | |
| D. | 溶液中大量存在的离子共有六种 |
| A. | NaAlO2 | B. | KAl(SO4)2•12H2O | C. | Al(OH)3 | D. | Al2O3 |
| A. | $\frac{a}{A+48}$(x-n)mol | B. | $\frac{a}{A+48}$(x-24-n)mol | C. | $\frac{a}{A+48}$(x+n)mol | D. | (x-n)mol |