题目内容
12.某高分子材料的结构如图所示: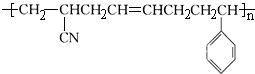 ,以下与此高分子材料相关的说法正确的是( )
,以下与此高分子材料相关的说法正确的是( )| A. | 合成该高分子材料的反应是缩聚反应 | |
| B. | 该高分子材料是由三种单体聚合而成的 | |
| C. | 合成该高分子材料的部分单体不能使溴水和酸性高锰酸钾溶液褪色 | |
| D. | 该高分子材料是体型结构高分子,具有热固性 |
分析 首先要根据高聚物的结构简式判断高聚物是加聚产物还是缩聚产物,然后根据推断单体的方法作出判断,
凡链节主链上只有碳原子并存在碳碳双键结构的高聚物,其规律是“见双键,四个碳,无双键,两个碳”画线断开,然后将半键闭合,即将单双键互换.
解答 解:链节中主碳链为8个碳原子,含有一个碳碳双键,单体为:CH2=CH-CN、CH2=CH-CH=CH2、C6H5-CH=CH2.
A.两端无端基原子,为加聚产物,故A错误;
B.该高分子材料是由三种单体:CH2=CH-CN、CH2=CH-CH=CH2、C6H5-CH=CH2,聚合而成的,故B正确;
C.三种单体中都含有碳碳双键,能使溴水和酸性高锰酸钾溶液褪色,故C错误;
D.该高分子材料是线型结构高分子,具有热塑性,故D错误.
故选B.
点评 本题考查了加聚反应原理、加聚反应产物单体的判断,题目难度中等,注意掌握加聚反应原理,能够根据高分子化合物结构简式判断其单体的结构简式.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
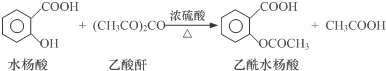
2.工业上常用水杨酸与乙酸酐反应制取解热镇痛药阿司匹林(乙酰水杨酸).
【反应原理】
【物质性质】
【实验流程】
(1)物质制备:向125mL的锥形瓶中依次加入4g水杨酸、10mL乙酸酐、0.5mL浓硫酸,振荡锥形瓶至水杨酸全部溶解,在85℃~90℃条件下,用热水浴加热5~10min.
①加入水杨酸、乙酸酐后,需缓慢滴加浓硫酸,否则产率会大大降低,其原因是水杨酸属于酚类物质,会被浓H2SO4氧化.
②控制反应温度85℃~90℃的原因既保证有较高的反应速率又减少了物质的挥发.
(2)产品结晶:取出锥形瓶,加入50mL蒸馏水冷却.待晶体完全析出后用布氏漏斗抽滤,再洗涤晶体,抽干.简要叙述如何洗涤布氏漏斗中的晶体?向布氏漏斗中加入冰水至浸没所有晶体,再抽滤,重复2~3次.
(3)产品提纯:将粗产品转移至150mL烧杯中,向其中慢慢加入试剂X并不断搅拌至不再产生气泡为止.进一步提纯最终获得乙酰水杨酸3.6g.
①试剂X为饱和碳酸钠溶液.
②实验中乙酰水杨酸的产率为69%(已知:水杨酸、乙酰水杨酸的相对分子质量分别为138和180).
(4)纯度检验:取少许产品加入盛有5mL水的试管中,加入1~2滴FeCl3溶液,溶液呈浅紫色,其可能的原因是产品中仍然可能含有水杨酸.
【反应原理】

【物质性质】
| 试剂 | 沸点(℃) | 溶解度 | 化学性质 |
| 水杨酸 | 211 | 微溶于冷水,易溶于热水 | |
| 乙酸酐 | 139 | 在水中逐渐分解 | |
| 乙酰水杨酸 | 微溶于水 | 与碳酸钠反应生成水溶性盐 |
(1)物质制备:向125mL的锥形瓶中依次加入4g水杨酸、10mL乙酸酐、0.5mL浓硫酸,振荡锥形瓶至水杨酸全部溶解,在85℃~90℃条件下,用热水浴加热5~10min.
①加入水杨酸、乙酸酐后,需缓慢滴加浓硫酸,否则产率会大大降低,其原因是水杨酸属于酚类物质,会被浓H2SO4氧化.
②控制反应温度85℃~90℃的原因既保证有较高的反应速率又减少了物质的挥发.
(2)产品结晶:取出锥形瓶,加入50mL蒸馏水冷却.待晶体完全析出后用布氏漏斗抽滤,再洗涤晶体,抽干.简要叙述如何洗涤布氏漏斗中的晶体?向布氏漏斗中加入冰水至浸没所有晶体,再抽滤,重复2~3次.
(3)产品提纯:将粗产品转移至150mL烧杯中,向其中慢慢加入试剂X并不断搅拌至不再产生气泡为止.进一步提纯最终获得乙酰水杨酸3.6g.
①试剂X为饱和碳酸钠溶液.
②实验中乙酰水杨酸的产率为69%(已知:水杨酸、乙酰水杨酸的相对分子质量分别为138和180).
(4)纯度检验:取少许产品加入盛有5mL水的试管中,加入1~2滴FeCl3溶液,溶液呈浅紫色,其可能的原因是产品中仍然可能含有水杨酸.
20.在平面形分子ClCH=CHCl中,C-Cl键采用的成键轨道是( )
| A. | sp-s | B. | sp2-s | C. | sp2-p | D. | sp3-s |
17.设NA为阿佛加德罗常数,下列叙述中正确的是( )
| A. | 22.4LH2 中含分子数为NA | |
| B. | 46gNO2 和N2O4混合气体中含有原子数为3NA | |
| C. | 1L1mol/L氨水溶液中离子总数为2NA | |
| D. | 1L2mol/L氯化铵溶液中有2NA个NH4+离子 |
4.将3.2g Cu与足量的浓硫酸在加热条件下充分反应.
(1)被还原的硫酸的物质的量为0.05mol.
(2)把反应后的溶液稀释至500ml,取出50ml,向其中加入足量的BaCl2溶液,得到沉淀20.27g,则稀释后所得溶液中SO42-的物质的量浓度为1.74mol/L(保留两位小数).
(3)若浓硫酸中含溶质为a mol,投入足量的铜片并加热,充分反应后,被还原的硫酸的物质的量n(H2SO4)<0.5amol.
(4)将产生的气体缓慢通入100ml b mol/L的氢氧化钠溶液中,若反应物均无剩余,则b的取值范围为0.5≤b≤1.
(5)讨论b的取值范围及与之对应的溶液的溶质及其物质的量,将结果填于下表中
(1)被还原的硫酸的物质的量为0.05mol.
(2)把反应后的溶液稀释至500ml,取出50ml,向其中加入足量的BaCl2溶液,得到沉淀20.27g,则稀释后所得溶液中SO42-的物质的量浓度为1.74mol/L(保留两位小数).
(3)若浓硫酸中含溶质为a mol,投入足量的铜片并加热,充分反应后,被还原的硫酸的物质的量n(H2SO4)<0.5amol.
(4)将产生的气体缓慢通入100ml b mol/L的氢氧化钠溶液中,若反应物均无剩余,则b的取值范围为0.5≤b≤1.
(5)讨论b的取值范围及与之对应的溶液的溶质及其物质的量,将结果填于下表中
| b的范围 | 溶质的种类 | 溶质的物质的量(mol) |
| 0.5 | NaHSO3 | 0.05 |
2.下列物质中,能使蛋白质变性的是( )
| A. | K2SO4 | B. | 福尔马林 | C. | NH4Cl | D. | Hg(NO3)2 |
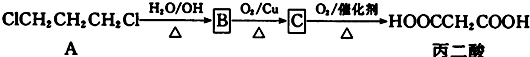

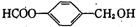 .
.