题目内容
【题目】制造一次性医用口罩的原料之一丙烯是三大合成材料的基本原料,丙烷脱氢作为一条增产丙烯的非化石燃料路线具有极其重要的现实意义。丙烷脱氢技术主要分为直接脱氢和氧化脱氢两种。
(1)根据下表提供的数据,计算丙烷直接脱氢制丙烯的反应C3H8(g)![]() C3H6(g) +H2(g)的H=___。
C3H6(g) +H2(g)的H=___。
共价键 | C-C | C=C | C-H | H-H |
键能/(kJmol-1) | 348 | 615 | 413 | 436 |
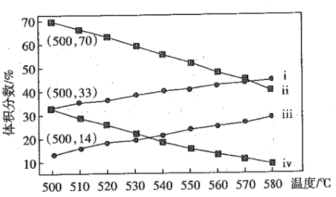
(2)下图为丙烷直接脱氢制丙烯反应中丙烷和丙烯的平衡体积分数与温度、压强的关系(图中压强分别为1×104Pa和1×105Pa)
①在恒容密闭容器中,下列情况能说明该反应达到平衡状态的是__(填字母)。
A.H保持不变
B.混合气体的密度保持不变
C.混合气体的平均摩尔质量保持不变
D.单位时间内生成1molH-H键,同时生成1molC=C键
②欲使丙烯的平衡产率提高,下列措施可行的是____(填字母)
A.增大压强 B.升高温度 C.保持容积不变充入氩气
工业生产中为提高丙烯的产率,还常在恒压时向原料气中掺入水蒸气,其目的是_____。
③1×104Pa时,图中表示丙烷和丙烯体积分数的曲线分别是___、____(填标号)
④1×104Pa、500℃时,该反应的平衡常数Kp=____Pa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,计算结果保留两位有效数字)
(3)利用CO2的弱氧化性,科学家开发了丙烷氧化脱氢制丙烯的新工艺,该工艺可采用铬的氧化物作催化剂,已知C3H8+CO2(g) C3H6(g)+CO(g)+H2O(l),该工艺可以有效消除催化剂表面的积炭,维持催化剂的活性,其原因是____,相对于丙烷直接裂解脱氢制丙烯的缺点是_____。
C3H6(g)+CO(g)+H2O(l),该工艺可以有效消除催化剂表面的积炭,维持催化剂的活性,其原因是____,相对于丙烷直接裂解脱氢制丙烯的缺点是_____。
【答案】+123 kJmol-1 C B 该反应是气体分子数增多的反应,恒压条件下充入水蒸气容器体积增大,平衡右移 ⅳ ⅰ 3.3×103 C与CO2反应生成CO,脱离催化剂表面 生成有毒气体CO(或其他合理说法)
【解析】
(1)比较丙烷与丙烯的结构,可确定断裂2个C-H键和1个C-C键,形成1个C=C键和1个H-H键,利用表中键能可计算C3H8(g)![]() C3H6(g) +H2(g)的H。
C3H6(g) +H2(g)的H。
(2)①A.对于一个化学反应,方程式确定后,H确定,与反应进行的程度无关;
B.混合气体的质量和体积都不变,密度始终不变;
C.混合气体的质量不变,物质的量增大,平均摩尔质量不断减小;
D.反应发生后,总是存在单位时间内生成1molH-H键,同时生成1molC=C键。
②A.增大压强,平衡逆向移动;
B.升高温度,平衡正向移动;
C.保持容积不变充入氩气,平衡不受影响。
工业生产中为提高丙烯的产率,还常在恒压时向原料气中掺入水蒸气,可增大混合气的体积,减小与反应有关气体的浓度。
③1×104Pa与1×105Pa进行对比,从平衡移动的方向确定图中表示丙烷和丙烯体积分数的曲线。
④1×104Pa、500℃时,丙烷、丙烯、氢气的体积分数都为33.3%,由此可计算该反应的平衡常数Kp。
(3) CO2具有氧化性,能与催化剂表面的积炭发生反应生成一氧化碳气体,由此可确定原因及缺点。
(1)比较丙烷与丙烯的结构,可确定断裂2个C-H键和1个C-C键,形成1个C=C键和1个H-H键,利用表中键能可计算C3H8(g)![]() C3H6(g) +H2(g)的H=(2×413+348) kJmol-1-(615+436) kJmol-1=+123 kJmol-1。答案为:+123 kJmol-1;
C3H6(g) +H2(g)的H=(2×413+348) kJmol-1-(615+436) kJmol-1=+123 kJmol-1。答案为:+123 kJmol-1;
(2)①A.对于一个化学反应,方程式确定后,H确定,与反应进行的程度无关,A不合题意;
B.混合气体的质量和体积都不变,密度始终不变,所以密度不变时不一定达平衡状态,B不合题意;
C.混合气体的质量不变,物质的量增大,平均摩尔质量不断减小,当平均摩尔质量不变时,反应达平衡状态,C符合题意;
D.反应发生后,总是存在单位时间内生成1molH-H键,同时生成1molC=C键,反应不一定达平衡状态,D不合题意;
故选C。答案为:C;
②A.增大压强,平衡逆向移动,丙烯的平衡产率减小,A不合题意;
B.升高温度,平衡正向移动,丙烯的平衡产率增大,B符合题意;
C.保持容积不变充入氩气,平衡不受影响,C不合题意;
故选B。答案为:B;
工业生产中为提高丙烯的产率,还常在恒压时向原料气中掺入水蒸气,可增大混合气的体积,减小与反应有关气体的浓度,其目的是该反应为气体分子数增多的反应,恒压条件下充入水蒸气容器体积增大,平衡右移。答案为:该反应是气体分子数增多的反应,恒压条件下充入水蒸气容器体积增大,平衡右移;
③升高温度,平衡正向移动,丙烷的体积分数减小,丙烯的体积分数增大,则ⅰ、ⅲ为丙烷的曲线,ⅱ、ⅳ为丙烯的曲线,1×104Pa与1×105Pa相比,压强减小,平衡正向移动,从而得出表示丙烷体积分数的曲线为ⅳ,表示丙烯体积分数的曲线为ⅰ。答案为:ⅳ;ⅰ;
④1×104Pa、500℃时,丙烷、丙烯、氢气的体积分数都为33.3%,由此可计算该反应的平衡常数Kp=![]() =3.3×103。答案:3.3×103;
=3.3×103。答案:3.3×103;
(3) CO2具有氧化性,能与催化剂表面的积炭发生反应生成一氧化碳气体,其原因是C与CO2反应生成CO,脱离催化剂表面;相对于丙烷直接裂解脱氢制丙烯的缺点是生成有毒气体CO(或其他合理说法)。答案为:C与CO2反应生成CO,脱离催化剂表面;生成有毒气体CO(或其他合理说法)。

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案