题目内容
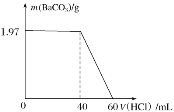
【题目】取Na2CO3和NaOH的混合液100mL,先向其中滴加Ba(OH)2溶液至不产生沉淀为止,再向其中滴加稀盐酸至沉淀消失,产生的沉淀的质量与消耗盐酸的体积如图所示:
(1)原混合液中Na2CO3与NaOH的物质的量浓度比为___。
(2)稀盐酸的物质的量浓度为___mol·L-1。
【答案】1:2 1
【解析】
在100mL Na2CO3和NaOH的混合液中滴加Ba(OH)2溶液至不产生沉淀为止,此时混合液中含有BaCO3沉淀和NaOH,再滴加稀盐酸至沉淀消失,其中前40mL盐酸中和NaOH,后20mL盐酸溶解BaCO3沉淀,结合原子守恒和电荷守恒即可解题。
(1)设原混合液中Na2CO3的物质的量为amol,NaOH的物质的量为bmol,则滴加滴加Ba(OH)2溶液至不产生沉淀为止时溶液中总NaOH的物质的量为(2a+b)mol;BaCO3的质量为1.97g,物质的量为![]() =0.01mol,由图示可知,20mL盐酸能溶解0.01molBaCO3,根据BaCO3+2H+=Ba2++H2O+CO2↑可知,20mL盐酸含n(HCl)=0.02mol, 故:2a=0.02、2a+b=0.04,解得:a=0.01,b=0.02,则原混合液中Na2CO3与NaOH的物质的量浓度比为0.01:0.02=1:2;
=0.01mol,由图示可知,20mL盐酸能溶解0.01molBaCO3,根据BaCO3+2H+=Ba2++H2O+CO2↑可知,20mL盐酸含n(HCl)=0.02mol, 故:2a=0.02、2a+b=0.04,解得:a=0.01,b=0.02,则原混合液中Na2CO3与NaOH的物质的量浓度比为0.01:0.02=1:2;
(2)盐酸的浓度为![]() =1mol/L。
=1mol/L。

【题目】现有常温下pH=2的HCl溶液甲和pH=2的CH3COOH溶液乙,请根据下列操作回答问题:
(1)常温下0.1mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是_____。
A.c(H+) B. c(H+)/c(CH3COOH) C.c(H+)·c(OH-)
(2)取10mL的乙溶液,加入等体积的水,CH3COOH的电离平衡________(填“向左”“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后溶液体积保持不变),待固体溶解后,溶液中的 c(H+)/c(CH3COOH) 比值将________(填“增大”“减小”或“无法确定”)。
(3)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗NaOH溶液体积的大小关系为V(甲)______(填“>”“<”或“=”)V(乙)。
(4)已知25℃时,下列酸的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | HClO | H2SO3 |
电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=4.7×10-11 | 3.0×10-8 | K1=1.54×10-2 K2=1.02×10-7 |
①下列微粒可以大量共存的是______![]() 填字母
填字母![]() 。
。
a.CO32-、HSO3- b.HCO3-、HSO3-
c.SO32-、HCO3- d.CO32- 、H2CO3
②写出下列反应的离子方程式:
H2SO3+Na2CO3(少量):_______________
室温下,0.1 mol·L-l的KOH溶液滴10.00mL 0.10 mol·L-l H2C2O4 (二元弱酸)溶液,所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。请回答下列问题:
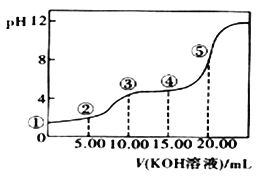
(5)点④所示溶液中:c(K+)+c(H2C2O4)+c(HC2O4)+c(C2O42)=_____mol/L。点⑤所示的溶液中各离子浓度的大小顺序_____.
(6)草酸晶体(H2C2O4·2H2O)为无色,某同学设计实验测定其纯度。实验过程如下:称取mg草酸晶体于锥形瓶中,加水完全溶解用cmol·L-1酸性KMnO4标准溶液进行滴定,则达到滴定终点时的现象是_______;该过程中发生反应的离子方程式为________;滴定过程中消耗VmLKMnO4标准溶液,草酸晶体纯度为________。
【题目】制造一次性医用口罩的原料之一丙烯是三大合成材料的基本原料,丙烷脱氢作为一条增产丙烯的非化石燃料路线具有极其重要的现实意义。丙烷脱氢技术主要分为直接脱氢和氧化脱氢两种。
(1)根据下表提供的数据,计算丙烷直接脱氢制丙烯的反应C3H8(g)![]() C3H6(g) +H2(g)的H=___。
C3H6(g) +H2(g)的H=___。
共价键 | C-C | C=C | C-H | H-H |
键能/(kJmol-1) | 348 | 615 | 413 | 436 |
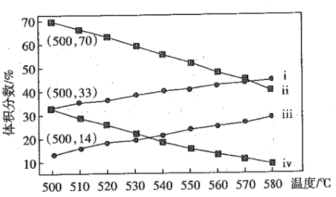
(2)下图为丙烷直接脱氢制丙烯反应中丙烷和丙烯的平衡体积分数与温度、压强的关系(图中压强分别为1×104Pa和1×105Pa)
①在恒容密闭容器中,下列情况能说明该反应达到平衡状态的是__(填字母)。
A.H保持不变
B.混合气体的密度保持不变
C.混合气体的平均摩尔质量保持不变
D.单位时间内生成1molH-H键,同时生成1molC=C键
②欲使丙烯的平衡产率提高,下列措施可行的是____(填字母)
A.增大压强 B.升高温度 C.保持容积不变充入氩气
工业生产中为提高丙烯的产率,还常在恒压时向原料气中掺入水蒸气,其目的是_____。
③1×104Pa时,图中表示丙烷和丙烯体积分数的曲线分别是___、____(填标号)
④1×104Pa、500℃时,该反应的平衡常数Kp=____Pa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,计算结果保留两位有效数字)
(3)利用CO2的弱氧化性,科学家开发了丙烷氧化脱氢制丙烯的新工艺,该工艺可采用铬的氧化物作催化剂,已知C3H8+CO2(g) C3H6(g)+CO(g)+H2O(l),该工艺可以有效消除催化剂表面的积炭,维持催化剂的活性,其原因是____,相对于丙烷直接裂解脱氢制丙烯的缺点是_____。
C3H6(g)+CO(g)+H2O(l),该工艺可以有效消除催化剂表面的积炭,维持催化剂的活性,其原因是____,相对于丙烷直接裂解脱氢制丙烯的缺点是_____。