题目内容
【题目】Fe3+与SCN-形成的配离子颜色极似血液,常被用于电影特技和魔术表演。回答下列问题:
(1)写出Fe3+的电子排布式:___________;SCN-的结构式为________
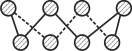
(2)基态硫原子中,核外占据最高能级电子的电子云轮廓图形状为_________。硫的一种同素异形体分子式为S8,其结构如图所示,其中S原子的杂化轨道类型为______。S8易溶于二硫化碳的原因是__________________________________________________。
(3)已知立方氮化硼晶体内存在配位键,则其晶体中配位键与普通共价键数目之比为______。原子坐标参数可表示晶胞内部各原子的相对位置,图中a处B的原子坐标参数为(0, 0, 0),则距离该B原子最近的N原子坐标参数为_________。
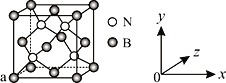
(4)单质铁的晶体结构如图所示,该堆积方式名称为________。已知该晶胞的密度为ρ g/cm3,则铁原子半径的计算式为______________ pm。

【答案】1s22s22p63s23p63d5或[Ar]3d5 [S-C≡N]-或[S=C=N]- 哑铃形 sp3 S8和二硫化碳都是非极性分子,由相似相溶原理S8易溶于二硫化碳 1:3 (![]() ,
,![]() ,
,![]() ) 体心立方堆积
) 体心立方堆积 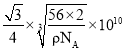
【解析】
(1)Fe3+的外围电子排布为3d5,结合泡利原理、洪特规则画出排布图为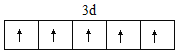 ;SCN-与CO2互为等电子体,二者结构相似,SCN-结构式为[S-C≡N]-或[S=C=N]-,SCN-中σ键与π键数目之比,2:2=1:1;
;SCN-与CO2互为等电子体,二者结构相似,SCN-结构式为[S-C≡N]-或[S=C=N]-,SCN-中σ键与π键数目之比,2:2=1:1;
(2)基态S原子核外电子排布式为1s22s22p63s23p4,其最高能级的电子为3p电子,电子云为哑铃形;S原子形成2个S-S键、还有2对孤电子对,杂化轨道数目为4,为sp3杂化;S8、CS2都是非极性分子,根据相似相溶知,S8易溶于二硫化碳;
(3)硼原子价电子数为3,形成4个共价键,有1个配位键、3个普通化学键;a处B的原子坐标参数为(0,0,0),距离该B原子最近的N原子连线处于晶胞体对角线上,且二者距离为体对角线的![]() ,则该N原子到各坐标平面距离均等于晶胞棱长的
,则该N原子到各坐标平面距离均等于晶胞棱长的![]() ,故该坐标为(
,故该坐标为(![]() ,
,![]() ,
,![]() );
);
(4)该堆积方式为体心立方堆积,该晶胞中Fe原子个数=1+8×![]() =2,体对角线上3个原子紧密相邻,晶胞棱长=
=2,体对角线上3个原子紧密相邻,晶胞棱长=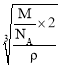 ,体心立方堆积中原子半径=
,体心立方堆积中原子半径=![]() ×棱长,所以铁原子半径=
×棱长,所以铁原子半径= 。
。

【题目】工业上CO2、CH4等含碳化合物有着重要的应用。
(1)科学家以CH4为原料来制备乙烯,同时得到氢气。已知相关物质的标准燃烧热如下表所示,写出甲烷制备乙烯的热化学方程式:__。
物质 | 标准燃烧热/kJ·mol-1 |
氢气 | -285.8 |
甲烷 | -890.3 |
乙烯 | -1411.0 |
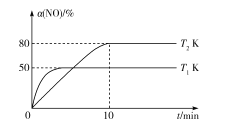
(2)在400℃时,向初始体积为1L的恒容密闭反应器中充入1molCH4,发生上述反应,测得平衡混合气体中C2H4的体积分数为20.0%。
①该温度下,平衡常数K=__。
②若向该平衡体系中充入等物质的量的CH4和H2,则平衡将___(填“正向移动”或“逆向移动”或“不移动”成“无法确定”),理由是__。
(3)科学家用氮化镓材料与铜组装成如图所示的人工光合系统实现CO2的再利用。
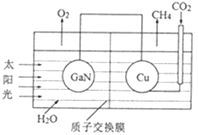
①该电化学装置属于__(填“原电池”或“电解池”)。
②该电池的Cu电极上发生反应的电极方程式为__。