题目内容
(10分)在一容积为2 L的密闭容器中加入2 molA和3 molB,保持温度为30℃,在催化剂存在的条件下进行下列反应:A(g)+2B(g)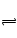 3C(g),达到平衡后生成1.5 mol C,此时,平衡混合气中C的体积分数为ω;若将温度升高到70℃后,其他条件均不变,当反应重新达到平衡时,C的物质的量为1.2 mol。
3C(g),达到平衡后生成1.5 mol C,此时,平衡混合气中C的体积分数为ω;若将温度升高到70℃后,其他条件均不变,当反应重新达到平衡时,C的物质的量为1.2 mol。
请回答下列问题,
(1)该反应的焓变△H 0(填“>”、“<”或“=”)。
(2)30℃时,平衡混合气中C的体积分数ω= ,A物质的转化率与B物质的转化率之比为 。
(3)30℃时,若在同一容器中加入1.5 mol A、 mol B和1.5 mol C,则平衡混合气中C的体积分数仍为ω,此时平衡体系中A的物质的量浓度为 mol·L-1。
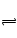 3C(g),达到平衡后生成1.5 mol C,此时,平衡混合气中C的体积分数为ω;若将温度升高到70℃后,其他条件均不变,当反应重新达到平衡时,C的物质的量为1.2 mol。
3C(g),达到平衡后生成1.5 mol C,此时,平衡混合气中C的体积分数为ω;若将温度升高到70℃后,其他条件均不变,当反应重新达到平衡时,C的物质的量为1.2 mol。请回答下列问题,
(1)该反应的焓变△H 0(填“>”、“<”或“=”)。
(2)30℃时,平衡混合气中C的体积分数ω= ,A物质的转化率与B物质的转化率之比为 。
(3)30℃时,若在同一容器中加入1.5 mol A、 mol B和1.5 mol C,则平衡混合气中C的体积分数仍为ω,此时平衡体系中A的物质的量浓度为 mol·L-1。
(1) < (2) 30% 3/4 (3) 2 0.75
(1)升高温度,生成物的物质的量减少,说明平衡向泥反应方向移动,因此正反应是放热反应,即△H小于0。
(2)因为反应前后体积不变,所以平衡混合气中C的体积分数ω=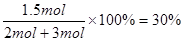 。生成1.5 mol C,消耗A和B的物质的量分别是0.5mol和1.0mol,所以A和B的转化率之比是
。生成1.5 mol C,消耗A和B的物质的量分别是0.5mol和1.0mol,所以A和B的转化率之比是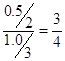 。
。
(3)根据条件可知,这是一个等效平衡。由于反应前后是体积不变的,所以要使平衡等效,则C的物质的量全部转化为A和B之和,A、B的物质的量之比应等于2︰3,1.5molC可以生成0.5mol和1.0molB,所以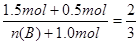 ,解得B的物质的量是2mol。因为平衡等效,所以根据(2)可知平衡体系中A的物质的量浓度为
,解得B的物质的量是2mol。因为平衡等效,所以根据(2)可知平衡体系中A的物质的量浓度为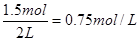 。
。
(2)因为反应前后体积不变,所以平衡混合气中C的体积分数ω=
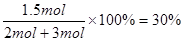 。生成1.5 mol C,消耗A和B的物质的量分别是0.5mol和1.0mol,所以A和B的转化率之比是
。生成1.5 mol C,消耗A和B的物质的量分别是0.5mol和1.0mol,所以A和B的转化率之比是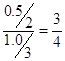 。
。(3)根据条件可知,这是一个等效平衡。由于反应前后是体积不变的,所以要使平衡等效,则C的物质的量全部转化为A和B之和,A、B的物质的量之比应等于2︰3,1.5molC可以生成0.5mol和1.0molB,所以
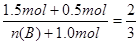 ,解得B的物质的量是2mol。因为平衡等效,所以根据(2)可知平衡体系中A的物质的量浓度为
,解得B的物质的量是2mol。因为平衡等效,所以根据(2)可知平衡体系中A的物质的量浓度为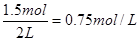 。
。
练习册系列答案
相关题目
 pC(g);△H<0中m、n、p为系数,且m+n>p。分析下列各图,在平衡体系中A的质量分数与温度t℃、压强P关系正确的是( )
pC(g);△H<0中m、n、p为系数,且m+n>p。分析下列各图,在平衡体系中A的质量分数与温度t℃、压强P关系正确的是( )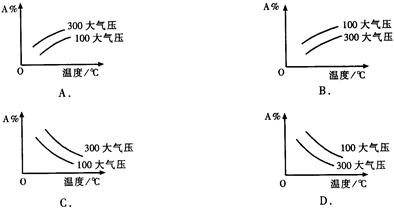
 2NH3。达到平衡后,测得反应放出的热量为18.4kJ,混合气体的物质的量为3.6mol,容器内的压强变为原来的90%。
2NH3。达到平衡后,测得反应放出的热量为18.4kJ,混合气体的物质的量为3.6mol,容器内的压强变为原来的90%。 ?2SO3(g) ΔH=-190kJ·mol-1
?2SO3(g) ΔH=-190kJ·mol-1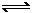 ?N2O4。反应中测得相关数据如下表所示:
?N2O4。反应中测得相关数据如下表所示: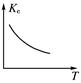
 2NH3
2NH3 C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列正确的是( )
C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列正确的是( ) 2SO3(g),此时容器中SO3的浓度为0.9mol/L,O2的物质的量为2.1mol,试求:① SO2的转化率;② O2的起始浓度(mol/L);③ SO2的平均反应速率(mol/L· min)
2SO3(g),此时容器中SO3的浓度为0.9mol/L,O2的物质的量为2.1mol,试求:① SO2的转化率;② O2的起始浓度(mol/L);③ SO2的平均反应速率(mol/L· min)  2C(g) ΔH >0,下列图象中正确的是
2C(g) ΔH >0,下列图象中正确的是