题目内容
对于可逆反应A(g)+2B(g)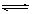 2C(g)(正反应吸热),下列图象中正确的是
2C(g)(正反应吸热),下列图象中正确的是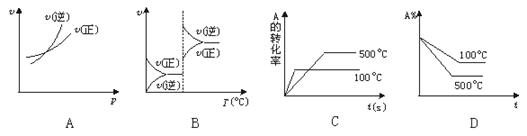
D
解析试题分析:A. 由于正反应是气体体积减小的反应,当反应达到平衡后,增大压强,平衡向正反应方向移动,而图像A是向逆反应方向移动,错误;B该反应的正反应是吸热反应,当升高温度后,平衡向吸热反应方向移动,所以升高温度平衡向正反应方向移动,而图像B是向逆反应方向移动,错误;C.升高温度,化学反应速率加快,首先达到平衡,而图像C是后达到平衡,错误;D.升高温度平衡向吸热反应方向移动,即向正反应方向移动,所以A的平衡含量减小,故该选项D正确。
考点:考查图像法在化学反应速率、化学平衡、物质的平衡含量的影响的知识。

 应用题作业本系列答案
应用题作业本系列答案在密闭容器中进行反应:X(g)+3Y(g) 2Z(g),有关下列图像的说法正确的是
2Z(g),有关下列图像的说法正确的是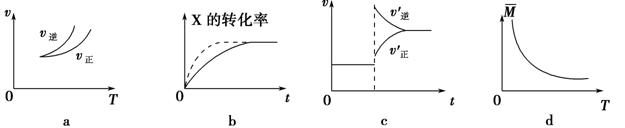
| A.依据图a可判断正反应为吸热反应 |
| B.在图b中,虚线可表示压强增大 |
| C.若正反应的ΔH<0,图c可表示升高温度使平衡向逆反应方向移动 |
| D.由图d中气体平均相对分子质量随温度的变化情况,可推知正反应的ΔH>0 |
已知2SO2 (g)+O2 (g)  2SO3 (g);△H =﹣197kJ?mol﹣1,向同温、同体积的三个密闭容器中分别充入气体,起始投料量如下表:
2SO3 (g);△H =﹣197kJ?mol﹣1,向同温、同体积的三个密闭容器中分别充入气体,起始投料量如下表:
| | SO2 (mol) | O2 (mol) | SO3 (mol) |
| 甲 | 2 | 1 | 0 |
| 乙 | 4 | 2 | 0 |
| 丙 | 0 | 0 | 2 |
恒温、恒容下反应达平衡时,下列关系一定正确的是
A.SO3的质量m:2m甲 = m乙
B.容器内压强P:2P丙 > P乙
C.反应放出或吸收热量的数值Q:Q甲 > Q丙
D.c(SO2)与c(O2)之比a:a丙 > a乙
下列说法正确的是
| A.增大压强,使单位体积内活化分子数目增加,化学反应速率一定增大 |
| B.升高温度,使活化分子百分数增加,化学反应速率一定增大 |
| C.活化分子间所发生的分子间的碰撞均为有效碰撞 |
| D.加入反应物,使活化分子百分数增加,化学反应速率一定增大 |
下列措施对增大反应速率明显有效的是( )
| A.Na与无水乙醇反应时增大无水乙醇的用量 |
| B.Zn与25%的稀硫酸反应制取H2时,改用98%的浓硫酸 |
| C.在K2SO4与BaCl2两溶液反应时,增大压强 |
| D.将炭块磨成炭粉用于燃烧 |
一定条件下,可逆反应N2 + 3H2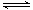 2NH3达到化学平衡状态,下列说法一定正确的是( )
2NH3达到化学平衡状态,下列说法一定正确的是( )
| A.每1 mol N≡N断裂的同时有2 mol N—H生成 |
| B.N2、H2、NH3的浓度之比为1:3:2 |
| C.N2减少的速率和NH3减少的速率之比为1:2 |
D.气体体积为初始体积的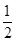 |
已知N2(g)+3H2(g) 2NH3(g) △H="—92.4" KJ/mol。在一恒温恒压的密闭容器里充入2mol N2和8mol H2达到平衡时生成1 mol NH3。现在相同条件下的同一容器中充入x mol N2,y mol H2和2 mol NH3,达到平衡时,NH3的质量分数与原来相同,且放出热量46.2KJ。则x、y的值分别为( )
2NH3(g) △H="—92.4" KJ/mol。在一恒温恒压的密闭容器里充入2mol N2和8mol H2达到平衡时生成1 mol NH3。现在相同条件下的同一容器中充入x mol N2,y mol H2和2 mol NH3,达到平衡时,NH3的质量分数与原来相同,且放出热量46.2KJ。则x、y的值分别为( )
| A.1.5, 6.5 | B.2, 8 | C.5, 21 | D.3, 13 |
用足量的铁片与一定量的稀硫酸反应制氢气,下列措施既能使氢气的生成速率加快,又不影响氢气的产量的是( )
| A.滴入适量Na2SO4溶液 | B.不用稀硫酸,改用98%的浓硫酸 |
| C.加入少量碳酸钠固体 | D.不用铁片,改用等质量的铁粉 |
对于反应2SO2+O2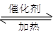 2SO3,下列判断正确的是
2SO3,下列判断正确的是
| A.2 mol SO2和足量的O2反应,一定生成2mol SO3 |
| B.平衡时SO2、O2、SO3的分子数之比为2∶1∶2 |
| C.平衡时SO2的消耗速率等于O2的生成速率的2倍 |
| D.平衡时SO2的浓度为O2浓度的2倍 |