题目内容
9.化学与资源、环境、生活关系密切,下列说法正确的是( )| A. | 硅的性质较稳定,在自然界中存在游离态的硅 | |
| B. | 陶瓷、水泥、玻璃、金刚砂均为传统无机非金属材料 | |
| C. | 水泥、普通玻璃的制备均要用到石灰石 | |
| D. | 高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱溶液无影响 |
分析 A.硅在自然界中以化合态存在;
B.传统无机非金属材料是指含有硅酸盐的材料;
C.根据工业上生产普通玻璃和水泥的原料判断;
D.二氧化硅为酸性氧化物,能够与强碱反应.
解答 解:A.硅在自然界中以化合态存在,自然界中无游离态的硅,故A错误;
B.金刚砂不含硅酸盐,不属于传统无机非金属材料,故B错误;
C.制玻璃的主要原料是纯碱、石灰石、石英,制水泥的主要原料是黏土、石灰石,均需要石灰石作为原料,故C正确;
D.二氧化硅为酸性氧化物,能够与强碱反应,光导纤维遇强碱溶液发生反应,会被破坏,故D错误;
故选:C.
点评 本题考查硅及其化合物的性质与用途、硅酸盐工业等,注意传统无机非金属材料的定义,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.有四个系列同族元素形成的物质,101.3kP时测定它们的沸点(℃)如表所示:
对应表中内容,下列叙述中不正确的是( )
| ① | He-268.8 | (a)-249.5 | Ar-185.8 | Kr 151.7 |
| ② | F2 -187.0 | Cl2 -33.6 | (b) 58.7 | I2 184.0 |
| ③ | (c) 19.4 | HCl-84.0 | HBr-67.0 | HI-35.3 |
| ④ | H2O 100.0 | H2S-60.0 | (d)-42.0 | H2Te-1.8 |
| A. | a、b、c、d的化学式分别为Ne、Br2、HF、H2Se | |
| B. | 系列②中各物质均只有强氧化性 | |
| C. | 系列④中各化合物的稳定性顺序为:H2O>H2S>d>H2Te | |
| D. | 系列③中各物质对应物质水溶液的酸性和还原性均逐渐增强 |
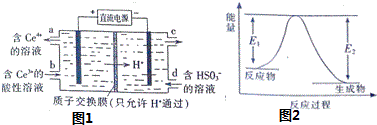
4.某同学将Fe+2FeCl3=3FeCl2设计成原电池装置如图所示.下列说法正确的是( )

| A. | 电子由铁极经溶液向铂极迁移 | |
| B. | 放电过程中交换膜右侧溶液颜色逐渐变浅 | |
| C. | 正极的电极反应式为Fe3++3e-=Fe | |
| D. | 若转移2mole-,交换膜右侧溶液中约减少3mol离子 |
14.下列各离子组在溶液中能大量共存且通入括号中相应气体后,仍能大量共存的是( )
| A. | NH4+、Ca2+、HSO3-、Cl- (氨气) | B. | Ba2+、NO3-、Na+、Cl- (二氧化硫) | ||
| C. | Na+、K+、HCO3-、Cl- (二氧化碳) | D. | Al3+、SO42-、HCO3-、NO3- (氯化氢) |
1.化学与生产、生活密切相关,下列说法错误的是( )
| A. | 铝需经过特别处理才具有抗腐蚀能力 | |
| B. | 洁厕剂和漂白精不能混合使用,否则易产生有毒气体 | |
| C. | Li是最轻的金属也是活动性很强的金属,是制造电池的理想物质 | |
| D. | 只要符合限量,“食用色素”、“亚硝酸盐”可以作为某些食品的添加剂 |
18.实验室常用于保存钠的液体是( )
| A. | 煤油 | B. | 水. | C. | 汽油 | D. | 四氯化碳 |
19.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 澄清透明的溶液中:MnO4-、SO42-、K+、Fe3+ | |
| B. | 0.1 mol•L-1FeCl3溶液中:Mg2+、NH4+、SCN-、SO42- | |
| C. | 滴入甲基橙显黄色的溶液中:Na+、ClO-、I-、SO42- | |
| D. | 水电离产生的c(H+)=10-12 mol•L-1的溶液中:K+、Na+、NO3-、CH3COO- |