题目内容
【题目】弱电解质的电离平衡、盐类的水解平衡均属于化学平衡。根据要求回答问題。
(1)一定温度下,向1 L 0.1 mol·L-1CH3COOH溶液中加入0.1 mol CH3COONa固体,则醋酸的电离平衡向________(填“正”或“逆”)反应方向移动;水的电离程度将________(填“增大”、“减小”或“不变”)。
(2)99℃时,KW=1.0×10-12 mol2·L-2,该温度下测得0.1 mol·L-1Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为______。
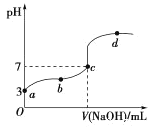
②体积相等、pH=1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气_____。
A.盐酸多 B.H2A多 C.一样多 D.无法确定
③将0.1 mol·L-1H2A溶液与0.2 mol·L-1氨水等体积混合,完全反应后溶液中各离子浓度的电荷守恒关系式为__________。
(3)已知常温下,H2SO3的电离常数为Kal=1.54×10-2,Ka2=1.02×10-7,H2CO3的电离常数为Kal=4.30×10-7,Ka2=5.60×10-11。
①下列微粒可以大量共存的是________(填字母)。
a.![]() 、
、![]() b.
b.![]() 、
、![]() c.
c.![]() 、
、![]() d.H2SO3、
d.H2SO3、![]()
②已知NaHSO3溶液显酸性,溶液中各离子浓度从大到小的排列顺序是_______。
(4)0.1 mol·L-1的NaHA溶液,测得溶液显碱性。则该溶液中 c(H2A)________c(A2-)(填“>”、“<”或“=”),作出此判断的依据是__________(用文字解释)。
【答案】逆 增大 H2A=2H++A2- C c(![]() )+c(H+)=2c(A2-)+c(OH-) bc c(Na+)>c(
)+c(H+)=2c(A2-)+c(OH-) bc c(Na+)>c(![]() )>c(H+)>c(
)>c(H+)>c(![]() )>c(OH-) > NaHA溶液显碱性,说明HA-水解程度大于电离程度
)>c(OH-) > NaHA溶液显碱性,说明HA-水解程度大于电离程度
【解析】
(1)同离子效应抑制弱电解质的电离;
(2)①由99℃时的KW计算中性时的pH=6,说明该溶液为中性,从而推出H2A为强酸;
②等pH、等体积的两种酸物质的量相同,产生的氢气也一样多;
③溶液存在电荷守恒;
(3)Ka越大,酸性越强,酸性较强的能与酸性较弱的酸根离子反应;
(4)NaHA溶液显碱性说明HA-水解程度大于电离程度。
(1)向CH3COOH中加入CH3COONa固体,CH3COONa电离导致溶液中c(CH3COO-)增大而抑制CH3COOH电离,则醋酸的电离平衡向逆反应方向移动;水的电离增大;故答案为:逆;增大;
(2)①99℃时,KW=1.0×10-12 mol2·L-2,纯水中![]() ,则pH为6,该温度下测得0.1 mol·L-1Na2A溶液的pH=6,说明该溶液为中性,即无离子发生水解,说明H2A是强酸,完全电离,电离方程式为:H2A=2H++A2-;
,则pH为6,该温度下测得0.1 mol·L-1Na2A溶液的pH=6,说明该溶液为中性,即无离子发生水解,说明H2A是强酸,完全电离,电离方程式为:H2A=2H++A2-;
②H2A是强酸,体积相等、pH=1的盐酸与H2A溶液中n(H+)相同,故两种酸与足量的Zn反应,产生的氢气一样多,故答案为:C;
③(NH4)2A在水中完全电离,根据电荷守恒:![]() ;
;
(3)①a.H2SO3的Ka2=1.02×10-7,H2CO3的Ka2=5.60×10-11,Ka越大,酸性越大,说明![]() 酸性比
酸性比![]() 的强,故
的强,故![]() 、
、![]() 不能大量共存,a错误;
不能大量共存,a错误;
b.由a项分析可知,![]() 、
、![]() 可以大量共存,b正确;
可以大量共存,b正确;
c.![]() 酸性比
酸性比![]() 的强,/span>
的强,/span>![]() 与
与![]() 不反应,能共存,c正确;
不反应,能共存,c正确;
d.H2SO3的Ka1大于H2CO3的Ka2,则H2SO3酸性比![]() 的强,两者能反应,不能共存,d错误;
的强,两者能反应,不能共存,d错误;
故答案选bc;
②NaHSO3溶液显酸性,说明![]() 电离程度大于水解程度,故离子浓度从大到小的排列顺序:c(Na+)>c(
电离程度大于水解程度,故离子浓度从大到小的排列顺序:c(Na+)>c(![]() )>c(H+)>c(
)>c(H+)>c(![]() )>c(OH-);
)>c(OH-);
(4)NaHA溶液显碱性,说明水解程度大于电离程度,故c(H2A)>c(A2-),判断的依据是:NaHA溶液显碱性,说明HA-水解程度大于电离程度,故答案为:>;NaHA溶液显碱性,说明HA-水解程度大于电离程度。

 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案【题目】向2 L的密闭容器中充入1mol A和1mol B,反应 A(g) + B(g)C(g) + D(g) ΔH的平衡常数(K)和温度(T)的关系如下:
温度/ ℃ | 700 | 800 | 900 |
平衡常数 | 0.1 | X | 1 |
800℃时,经5s反应达到平衡状态,此时B的平均反应速率v(B)=0.04 mol/(L·s)。下列说法不正确的是
A.平衡时,c(B)为0.6 mol·L-1
B.800℃时平衡常数X=4/9
C.ΔH >0
D.900℃该反应达到平衡状态时,A的物质的量为0.5 mol
【题目】下列有关实验操作、现象、解释或结论都正确的是
选项 | 实验操作 | 现象 | 解释或结论 |
A | 充分吸收了Na2SiO3 饱和溶液的小木条,沥干后放在酒精灯外焰加热 | 小木条不燃烧 | Na2SiO3 可作防火剂 |
B | 将 H2 在充满Cl2 的集气瓶中燃烧 | 集气瓶口上方有白烟生成 | H2、Cl2 化合生成HCl |
C | 将 SO2 通入酸性高锰酸钾溶液中 | 溶液褪色 | SO2 具有氧化性 |
D | 除去表面氧化膜的铝箔,在酒精灯上充分加热 | 铝不能滴落下来 | 铝熔点高,没能熔化 |
A.AB.BC.CD.D