题目内容
【题目】某铜钴矿石主要含有 CoO(OH)、CoCO3、Cu2(OH)2CO3 和 SiO2,及一定量的 Fe2O3、MgO 和CaO等。由该矿石制Co2O3的部分工艺流程如图:
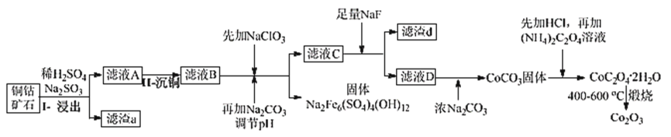
(1)在“浸出”过程中可以提高反应速率的方法有__。(写出两种即可)
(2)在“II-沉铜”过程中加入了FeS固体,得到更难溶的CuS,写出该步反应的离子方程式__。
(3)NaClO3 的主要作用是__。
(4)滤渣d 的主要成分是__。
(5)滤液D 中加入浓Na2CO3 后又加入HCl 溶解,其目的是__。
(6)写出CoC2O4·2H2O 在空气中煅烧得到 Co2O3 的化学方程式__。
【答案】升高温度或将矿石粉碎或适当增大硫酸的浓度等(只要两条即可) ![]() 将Fe2+氧化为Fe3+ MgF2、CaF2 富集Co2+ 4CoC2O42H2O+3O2
将Fe2+氧化为Fe3+ MgF2、CaF2 富集Co2+ 4CoC2O42H2O+3O2![]() 2Co2O3+8CO2↑+8H2O
2Co2O3+8CO2↑+8H2O
【解析】
铜钴矿中加入过量稀硫酸和Na2SO3,得到的滤液A含Co2+、Cu2+、Fe2+、Mg2+、Ca2+,加入的Na2SO3主要是将Co3+、Fe3+还原为Co2+、Fe2+,沉铜后加入NaClO3将Fe2+氧化为Fe3+,加入Na2CO3调pH,可以使Fe3+沉淀,过滤后所得滤液主要含有Co2+、Mg2+、Ca2+,再用NaF溶液除去钙离子、镁离子,过滤后,向滤液中加入浓Na2CO3溶液转为CoCO3固体,碳酸钴先用盐酸溶解、最后加入草酸铵溶液得到草酸钴,煅烧后制得Co2O3。
(1)“浸泡”过程中可以加快反应速率的方法是升温、粉碎矿石、适当增加稀硫酸浓度等;故答案为:升高温度、将矿石粉碎、适当增大硫酸的浓度等
(2)在“II-沉铜”过程中加入了FeS固体,得到更难溶的CuS,即Cu2+与FeS反应生成CuS和Fe2+,故该步反应的离子方程式为:![]() ,故答案为:
,故答案为:![]()
(3)由于铜钴矿中+3价的Fe3+被Na2SO3还原成了Fe2+,而加入NaClO3溶液后,再加入碳酸钠溶液调节pH得到了+3价的Na2Fe6(SO4)4(OH)12,故可推知加入NaClO3溶液能发生反应ClO3-+6Fe2++6H+═Cl-+6Fe3++3H2O,故主要目的是将Fe2+氧化为Fe3+;故答案为:将Fe2+氧化为Fe3+;
(4)由上述分析可知,滤液C中含有大量Ca2+、Mg2+,加入NaF后将转化成MgF2、CaF2,滤渣d 的主要成分是MgF2、CaF2,故答案为:MgF2、CaF2;
(5)滤液D中加入浓Na2CO3,将滤液中的Co2+转化为CoCO3沉淀后又加入HCl溶解生成Co2+再与草酸铵反应液,其目的是提高Co2+的浓度和纯度,故答案为:富集Co2+;
(6)由钴的化合价分析可知,CoC2O4·2H2O在空气中煅烧得到Co2O3的反应是一个氧化还原反应,故其化学方程式为4CoC2O42H2O+3O2![]() 2Co2O3+8CO2↑+8H2O,故答案为:4CoC2O42H2O+3O2
2Co2O3+8CO2↑+8H2O,故答案为:4CoC2O42H2O+3O2![]() 2Co2O3+8CO2↑+8H2O。
2Co2O3+8CO2↑+8H2O。