题目内容
【题目】硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得。已知:Na2S2O3在酸性溶液中不能稳定存在。
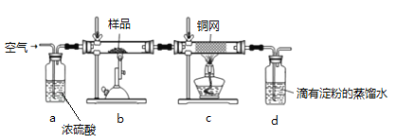
(1)某研究小组设计了制备Na2S2O3·5H2O的装置和部分操作步骤如图所示。
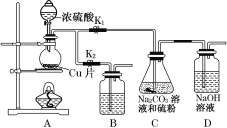
Ⅰ.打开K1,关闭K2,向圆底烧瓶中加入足量浓硫酸,加热。
Ⅱ.C中的混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少。当C中溶液的pH接近7时即停止C中的反应。
Ⅲ.过滤C中的混合液。
Ⅳ.将滤液加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品。
①步骤Ⅰ中,圆底烧瓶内发生反应的化学方程式是_________________。
②步骤Ⅱ中,“当C中溶液的pH接近7时即停止C中的反应”的原因是____________。“停止C中的反应”的操作是____________________________________。
③装置B中盛放的试剂是________溶液(填化学式),其作用是___________________。
(2)依据反应2S2O+I2=S4O+2I-,可用I2的标准溶液测定产品的纯度。取5.5 g产品,配制成100 mL溶液。取10 mL溶液,以淀粉溶液为指示剂,用浓度为0.050 mol·L-1的标准溶液进行滴定,相关数据记录如表所示。
编号 | 1 | 2 | 3 | 4 |
溶液的体积/mL | 10.00 | 10.00 | 10.00 | 10.00 |
消耗I2标准溶液的体积/mL | 19.99 | 19.98 | 17.13 | 20.03 |
①判断达到滴定终点的现象是__________________________________________。
②Na2S2O3·5H2O(式量M=248)在产品中的质量分数是(计算结果保留1位小数)________。
【答案】(1)①Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
② Na2S2O3在酸性溶液中不能稳定存在 打开K2,关闭K1
③ NaOH C中的反应停止后,吸收A中产生的多余SO2,防止空气污染
①加入最后一滴I2标准溶液后,溶液变蓝,且半分钟内颜色不改变 ②90.2%
【解析】
试题分析:(Ⅰ)①铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
②Na2S2O3在酸性溶液中不能稳定存在,因此“当C中溶液的pH接近7时即停止C中的反应”;二氧化硫通入碳酸钠溶液中反应生成亚硫酸钠和硫粉反应生成硫代硫酸钠,C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少,因此停止C中的反应的操作是应打开K2,关闭K1 ;
③为防止过量的二氧化硫污染性气体排放到空气中污染环境,装置B是利用氢氧化钠溶液吸收多余的二氧化硫气体;
(Ⅱ)①以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,终点现象为溶液变蓝色且半分钟内不褪色;
②根据表中数据可知,第三次实验中消耗I2标准溶液的体积偏小,舍去,则实际消耗I2标准溶液的体积的平均值是=![]() mL=20mL,则根据反应的方程式2S2O32-+I2→S4O62-+2I-可知样品中Na2S2O35H2O的物质的量是0.050mol/L×0.0200L×2×10=0.02mol,所以Na2S2O35H2O在产品中的质量分数=
mL=20mL,则根据反应的方程式2S2O32-+I2→S4O62-+2I-可知样品中Na2S2O35H2O的物质的量是0.050mol/L×0.0200L×2×10=0.02mol,所以Na2S2O35H2O在产品中的质量分数=![]() ×100%=90.2%。
×100%=90.2%。

 阅读快车系列答案
阅读快车系列答案