题目内容
2.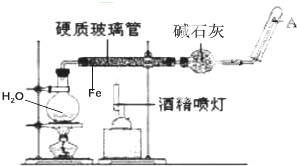 如图是在高温下,Fe与水蒸气的反应实验.
如图是在高温下,Fe与水蒸气的反应实验.请回答该实验中的问题:
(1)写出该反应的化学方程式:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
(2)圆底烧瓶中盛装的水,该装置在受热后的主要作用是:提供水蒸气;烧瓶底部放置了几片碎瓷片,其作用是:防止暴沸.
(3)碱石灰的作用是干燥生成的氢气.
(4)试管中收集的气体是氢气,如果在A处点燃该气体,则必须对其进行验纯.
分析 由图可知,圆底烧瓶中加热提供水蒸气,在硬质玻璃管中发生Fe与水蒸气的反应生成四氧化三铁和氢气,用碱石灰干燥氢气,在A中收集生成的氢气;注意加热液体时要防止暴沸,点燃可燃性气体前要检验气体的纯度.以此来解答.
解答 解:(1)圆底烧瓶中加热提供水蒸气,在硬质玻璃管中发生Fe与水蒸气的反应生成四氧化三铁和氢气,发生氧化还原反应:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,
故答案为3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
(2)圆底烧瓶中盛装的水,该装置在受热后的主要作用是:产生水蒸气;烧瓶底部放置了几片碎瓷片的目的是:防止暴沸;
故答案为:提供水蒸气;防止暴沸;
(3)圆底烧瓶中加热提供水蒸气,在硬质玻璃管中发生Fe与水蒸气的反应生成四氧化三铁和氢气,碱石灰用来干燥氢气,在A中收集纯净的氢气;
故答案为:干燥生成的氢气;
(4)水蒸气在硬质管中与铁粉反应生成的氢气,经碱石灰干燥后,在A中被收集;氢气的爆炸极限是4.0%~75.6%,即当氢气的含量在上述范围内时就会引起爆炸,因此,点燃氢气之前要检验纯度;点燃任何可燃性气体之前都要检验纯度,以防爆炸;
故答案为:氢气;验纯.
点评 本题考查性质实验的设计,涉及到实验基础知识,把握发生的反应及装置的作用、掌握实验安全知识为解答关键,难度不大.

练习册系列答案
相关题目
6.下列表示物质结构的化学用语正确的是( )
| A. | 氯化氢的电子式: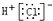 | B. | CO2的结构式:O=C=O | ||
| C. | 硫离子结构示意图: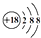 | D. | CCl4的电子式: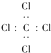 |
12.下列过程中,共价键被破坏的是( )
| A. | 碘升华 | B. | 溴蒸气被木炭吸附 | ||
| C. | 酒精溶于水 | D. | HCl气体溶于水 |