题目内容
在盛有足量M的体积可变的密容器中加入N,发生反应:M(s)+2N(g) 4P (g)+Q(g)
4P (g)+Q(g)
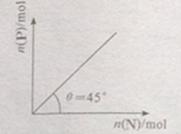
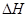 <0。在一定温度、压强下达到平衡,平衡时P的物质的量与起始时加入N的物质的量的变化关系如图所示。下列说法正确的是:
<0。在一定温度、压强下达到平衡,平衡时P的物质的量与起始时加入N的物质的量的变化关系如图所示。下列说法正确的是:
 4P (g)+Q(g)
4P (g)+Q(g)
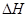 <0。在一定温度、压强下达到平衡,平衡时P的物质的量与起始时加入N的物质的量的变化关系如图所示。下列说法正确的是:
<0。在一定温度、压强下达到平衡,平衡时P的物质的量与起始时加入N的物质的量的变化关系如图所示。下列说法正确的是:
| A.平衡时N的转化率为50% |
B.当温度升高后,则图中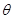 >45 >45 |
| C.若再加入N,则正、逆反应速率均逐渐增大 |
| D.若再加入N,则反应体系中气体密度减小 |
A
试题分析:A、根据图像结合方程式知,加入的N的物质的量与生成P的物质的量相等,所以该反应中有一半的N反应,所以N的转化率为50%,正确;B、压强一定,当升高温度时,平衡逆向移动,则P的物质的量会减少,由图可以看出
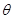 <45
<45 ,错误;C、因体积可变,再加入N时N的浓度不变,正、逆反应速率不变,错误;D、根据图像结合方程式知,加入的N的物质的量与生成P的物质的量相等,所以该反应中就有一半的N参加反应,根据方程式计算可得:只要温度不变,气体的平均摩尔质量就不变,所以若再加入N,再次达到平衡时体系气体密度始终不变,错误。
,错误;C、因体积可变,再加入N时N的浓度不变,正、逆反应速率不变,错误;D、根据图像结合方程式知,加入的N的物质的量与生成P的物质的量相等,所以该反应中就有一半的N参加反应,根据方程式计算可得:只要温度不变,气体的平均摩尔质量就不变,所以若再加入N,再次达到平衡时体系气体密度始终不变,错误。
练习册系列答案
相关题目
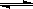 2Z(g); ΔH<0,达到平衡时,下列说法正确的是
2Z(g); ΔH<0,达到平衡时,下列说法正确的是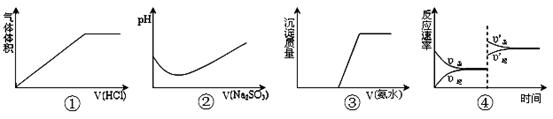
 2SO3 ΔH< 0 ,达平衡后,增大压强
2SO3 ΔH< 0 ,达平衡后,增大压强 2NO + O2 ΔH >0 达到平衡后,升温,混合气体的( )不变
2NO + O2 ΔH >0 达到平衡后,升温,混合气体的( )不变 CO2(g)+H2(g);CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如右图所示。下列说法错误的是
CO2(g)+H2(g);CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如右图所示。下列说法错误的是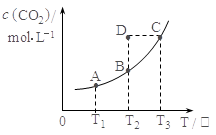
 CuS(s)+Mn2+(aq),下列说法错误的是 ( )
CuS(s)+Mn2+(aq),下列说法错误的是 ( )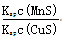
 N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时, N2O4的浓度为NO2的2倍,回答下列问题。
N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时, N2O4的浓度为NO2的2倍,回答下列问题。