题目内容
(18分)碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用。
(1)用于发射“天宫一号”的长征二号F火箭的燃料是液态偏二甲肼(CH3-NH-NH-CH3),氧化剂是液态四氧化二氮。二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,请写出该反应的热化学方程式________________________________________。
(2)298 K时,在2L的密闭容器中,发生可逆反应:2NO2(g) N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时, N2O4的浓度为NO2的2倍,回答下列问题。
N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时, N2O4的浓度为NO2的2倍,回答下列问题。

①298k时,该反应的平衡常数为________ L ·mol-1。
②下列事实能判断该反应处于平衡状态的是
a.混合气体的密度保持不变
b.混合气体的颜色不再变化
c. V(N2O4)正=2V(NO2)逆
③若反应在398K进行,某时刻测得n(NO2)="0.6" mol n(N2O4)=1.2mol,则此时
V(正) V(逆)(填“>”“<”或“=”)。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。
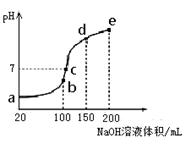
试分析图中a、b、c、d、e五个点,
①水的电离程度最大的是__________;
②其溶液中c(OH-)的数值最接近NH3·H2O的电离常
数K数值的是 ;
③在c点,溶液中各离子浓度由大到小的排列顺序
是__________。
(1)用于发射“天宫一号”的长征二号F火箭的燃料是液态偏二甲肼(CH3-NH-NH-CH3),氧化剂是液态四氧化二氮。二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,请写出该反应的热化学方程式________________________________________。
(2)298 K时,在2L的密闭容器中,发生可逆反应:2NO2(g)
 N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时, N2O4的浓度为NO2的2倍,回答下列问题。
N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时, N2O4的浓度为NO2的2倍,回答下列问题。
①298k时,该反应的平衡常数为________ L ·mol-1。
②下列事实能判断该反应处于平衡状态的是
a.混合气体的密度保持不变
b.混合气体的颜色不再变化
c. V(N2O4)正=2V(NO2)逆
③若反应在398K进行,某时刻测得n(NO2)="0.6" mol n(N2O4)=1.2mol,则此时
V(正) V(逆)(填“>”“<”或“=”)。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。

试分析图中a、b、c、d、e五个点,
①水的电离程度最大的是__________;
②其溶液中c(OH-)的数值最接近NH3·H2O的电离常
数K数值的是 ;
③在c点,溶液中各离子浓度由大到小的排列顺序
是__________。
(1)C2H8N2(l)+2N2O4(l)=2CO2(g)+3N2(g)+4H2O(l) ΔH=-2550 kJ·mol-1(3分)
(2)①6.67 (2分) ②b (2分) ③< (2分)
(3)①b (3分) ②d(3分) ③c(Na+)>c(SO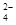 )>c(NH4+)>c(OH-)=c(H+)(3分)
)>c(NH4+)>c(OH-)=c(H+)(3分)
(2)①6.67 (2分) ②b (2分) ③< (2分)
(3)①b (3分) ②d(3分) ③c(Na+)>c(SO
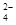 )>c(NH4+)>c(OH-)=c(H+)(3分)
)>c(NH4+)>c(OH-)=c(H+)(3分)试题分析:(1)根据题给信息和热化学方程式的书写原则知,室温下液态偏二甲肼和液态四氧化二氮反应的热化学方程式C2H8N2(l)+2N2O4(l)=2CO2(g)+3N2(g)+4H2O(l) ΔH=-2550 kJ·mol-1。(2)①根据题给图像知,298k时,N2O4的平衡浓度为0.6mol/L,N2O4的浓度为NO2的2倍,NO2的平衡浓度为0.3mol/L,该反应的平衡常数K=[N2O4]/[NO2]2=0.6/0.32="6.67" L ·mol-1。② a.反应在容积不变的容器中进行,由质量守恒定律知,混合气体的质量不变,混合气体的密度不随反应的进行而变化,不能作为平衡标志,错误; b.混合气体的颜色是由二氧化氮引起,混合气体的颜色不再变化,二氧化氮的浓度不变,已达平衡,正确; c. 由V(N2O4)正=2V(NO2)逆知,V(N2O4)正:V(NO2)逆=2,不等于化学计量数之比,错误,选b;③反应:2NO2(g)
 N2O4(g) ΔH=-a kJ·mol-1 (a>0)为放热反应,升高温度,平衡逆向移动,平衡常数减小,若反应在398K进行,平衡常数K<6.67 L ·mol-1,某时刻测得n(NO2)="0.6" mol n(N2O4)=1.2mol,则此时Q=c(N2O4)/c2(NO2)="6.67" L ·mol-1,Q>K,反应逆向进行,V(正)<V(逆)。(3)向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,发生的反应依次为:H++OH-
N2O4(g) ΔH=-a kJ·mol-1 (a>0)为放热反应,升高温度,平衡逆向移动,平衡常数减小,若反应在398K进行,平衡常数K<6.67 L ·mol-1,某时刻测得n(NO2)="0.6" mol n(N2O4)=1.2mol,则此时Q=c(N2O4)/c2(NO2)="6.67" L ·mol-1,Q>K,反应逆向进行,V(正)<V(逆)。(3)向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,发生的反应依次为:H++OH- H2O、NH4+ + OH-
H2O、NH4+ + OH- NH3·H2O。①当氢离子恰好完全反应时,溶液为硫酸钠和硫酸铵的混合物,水的电离程度最大,结合图像知,水的电离程度最大的是b;②Kb(NH3·H2O)=c(NH4+)c(OH-)/c(NH3·H2O),c(NH4+)与c(NH3·H2O)相等时,其溶液中c(OH-)的数值最接近NH3·H2O的电离常数K数值,结合题给图像知是d;③由图像知,c点溶液呈中性,溶液为硫酸钠、硫酸铵和一水合氨的混合液,各离子浓度由大到小的排列顺序是c(Na+)>c(SO
NH3·H2O。①当氢离子恰好完全反应时,溶液为硫酸钠和硫酸铵的混合物,水的电离程度最大,结合图像知,水的电离程度最大的是b;②Kb(NH3·H2O)=c(NH4+)c(OH-)/c(NH3·H2O),c(NH4+)与c(NH3·H2O)相等时,其溶液中c(OH-)的数值最接近NH3·H2O的电离常数K数值,结合题给图像知是d;③由图像知,c点溶液呈中性,溶液为硫酸钠、硫酸铵和一水合氨的混合液,各离子浓度由大到小的排列顺序是c(Na+)>c(SO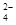 )>c(NH4+)>c(OH-)=c(H+)。
)>c(NH4+)>c(OH-)=c(H+)。
练习册系列答案
相关题目
 4P (g)+Q(g)
4P (g)+Q(g)
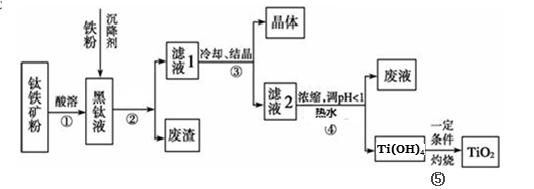
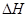 <0。在一定温度、压强下达到平衡,平衡时P的物质的量与起始时加入N的物质的量的变化关系如图所示。下列说法正确的是:
<0。在一定温度、压强下达到平衡,平衡时P的物质的量与起始时加入N的物质的量的变化关系如图所示。下列说法正确的是: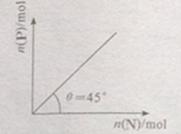
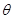 >45
>45
 3C(s) + 4NH3(g) ΔH>0,在700℃,CH4与N2在不同物质的量之比[n(CH4)/n(N2)]时CH4的平衡转化率如下图所示:
3C(s) + 4NH3(g) ΔH>0,在700℃,CH4与N2在不同物质的量之比[n(CH4)/n(N2)]时CH4的平衡转化率如下图所示: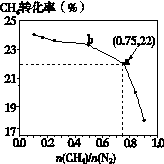
 CH3OH(g)
CH3OH(g) 2SO3(g),在一定条件下达到平衡,测得c(SO3)=0.04mol·L-1。以下表述正确的是
2SO3(g),在一定条件下达到平衡,测得c(SO3)=0.04mol·L-1。以下表述正确的是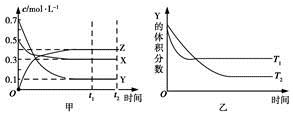
 2Z(g) ΔH>0
2Z(g) ΔH>0 CO2(g)+2H2O(g)
CO2(g)+2H2O(g)
 I2(g)+H2(g);△H>0,测得平衡时容器体积为1L,c(I2)=0.5mol/L。改变相关条件,下列结论正确的是
I2(g)+H2(g);△H>0,测得平衡时容器体积为1L,c(I2)=0.5mol/L。改变相关条件,下列结论正确的是