题目内容
黄铁矿主要成分是FeS2。某硫酸厂在进行黄铁矿成分测定时,取0.1000 g样品在空气中充分灼烧,将生成的SO2气体与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000 mol/L的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00 mL 。
已知:SO2 + 2Fe3+ + 2H2O→SO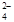 + 2Fe2+ + 4H+
+ 2Fe2+ + 4H+
Cr2O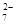 + 6 Fe2+ + 14 H+ →2 Cr3+ + 6 Fe3+ + 7 H2O
+ 6 Fe2+ + 14 H+ →2 Cr3+ + 6 Fe3+ + 7 H2O
(1)样品中FeS2的质量分数是(假设杂质不参加反应) 。
(2)若灼烧6 g FeS2产生的SO2全部转化为SO3气体时放出9.83 kJ热量,产生的SO3与水全部化合生成H2SO4,放出13.03kJ热量,写出SO3气体转化为H2SO4的热化学方程式: 。
(3)煅烧10 t上述黄铁矿,理论上产生SO2的体积(标准状况)为 ,制得98%的硫酸质量为 t ,SO2全部转化为H2SO4时放出的热量是 kJ。
(1)90.00%
(2)SO3(g)+H2O(1)═H2SO4(1);△H═-130.3 kJ/mol
(3).36×106;15;3.43×107
解析试题分析:
(1)取0.1000g样品在空气中充分灼烧,将生成的SO2气体与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000mol/L的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00mL。假设硫化亚铁物质的量为x,则3FeS2~6SO2~12Fe2+~2Cr2O72-
3 2
x 0.02000mol/l×0.02500L x=0.00075mol
所以样品中FeS2的质量分数=0.00075×120/0.1000×100%=90.00%
(2)灼烧6g FeS2产生的SO2全部转化为SO3气体时放出9.83kJ热量,依据硫元素守恒n(S)=2n(FeS2)=6g/120g.mol-1×2=0.1mol。产生的0.1molSO3与水全部化合生成H2SO4,放出13.03kJ热量,1molSO3与水全部化合生成H2SO4,放出130.3kJ,SO3气体转化为H2SO4的热化学方程式为:SO3(g)+H2O(1)═H2SO4(1);△H═-130.3 kJ/mol;故答案为:SO3(g)+H2O(1)═H2SO4(1);△H═-130.3 kJ/mol
(3)煅烧10t上述黄铁矿,含有FeS2的质量=10×106×90%=9×106g,物质的量= =7.5×104mol,依据硫元素守恒,理论上产生SO2的体积=7.5×104mol×2×22.4L/mol=3.36×106 L;理论上得到硫酸物质的量为7.5×104mol×2=1.5×105mol,质量=1.5×105mol×98g/mol=1.47×107g,制得98%的硫酸质量=
=7.5×104mol,依据硫元素守恒,理论上产生SO2的体积=7.5×104mol×2×22.4L/mol=3.36×106 L;理论上得到硫酸物质的量为7.5×104mol×2=1.5×105mol,质量=1.5×105mol×98g/mol=1.47×107g,制得98%的硫酸质量= =1.5×107g=15t。依据上题可知,0.1mol二氧化硫全部反应生成三氧化硫放热9.83kJ热量,产生的SO3与水全部化合生成H2SO4,放出13.03kJ热量,1.5×105molSO2全部转化为H2SO4时放出的热量=1.5×105mol×98.3KJ/mol+1.5×105mol×130.3KJ/mol=3.429×107KJ。故答案为:3.36×106;15;3.43×107。
=1.5×107g=15t。依据上题可知,0.1mol二氧化硫全部反应生成三氧化硫放热9.83kJ热量,产生的SO3与水全部化合生成H2SO4,放出13.03kJ热量,1.5×105molSO2全部转化为H2SO4时放出的热量=1.5×105mol×98.3KJ/mol+1.5×105mol×130.3KJ/mol=3.429×107KJ。故答案为:3.36×106;15;3.43×107。
考点:化学计算

 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。
(1)现有一种无色的鲜花营养液,可能由硝酸钙、碳酸钾、硝酸钾、氯化钾中的一种或几种物质组成,为探究其成分,某同学设计并完成了如下图所示的实验。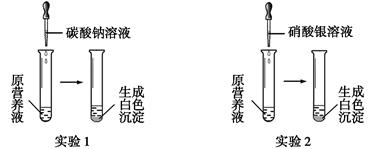
根据以上实验,请你填空。
①由实验1可确定原营养液中一定没有的物质是 (填化学式),写出生成白色沉淀的离子方程式是 。
②若测得原营养液中K+、Cl-的数目之比为2∶1,则原营养液是由 种溶质配制成的。
③某同学用氯化钙、硝酸钾、氯化钾配成的营养液中K+、Cl-、NO3-的数目之比为2∶5∶1,
则所用硝酸钾和氯化钙的物质的量之比是 。
(2)下表是500mL某“鲜花保鲜剂”中含有的成分,阅读后回答下列问题。
| 成分 | 质量(g) | 摩尔质量(g ·mol-1) |
| 蔗糖 | 68.4 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
①“鲜花保鲜剂”中蔗糖的物质的量浓度为___________________。
②配制该500mL “鲜花保鲜剂”所需的玻璃仪器除了烧杯、玻璃棒、量筒外还有 。
③在溶液配制过程中,下列操作能使配制结果偏小的是___________。
A.定容时仰视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.移液时,液体不小心从外壁流出
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
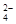 ,SO
,SO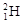 和
和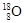 组成的水分子的物质的量 mol,其中含中子数为 mol,电子数为 个。
组成的水分子的物质的量 mol,其中含中子数为 mol,电子数为 个。 MnCl2+2H2O+Cl2↑。若0.1 molMnO4与足量的浓盐酸充分反应,则有 mol HCl被氧化,转移电子的物质的量为 mol,产生的Cl 2在标准状况下的体积为 L。
MnCl2+2H2O+Cl2↑。若0.1 molMnO4与足量的浓盐酸充分反应,则有 mol HCl被氧化,转移电子的物质的量为 mol,产生的Cl 2在标准状况下的体积为 L。