题目内容
(1)①现有11g由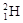 和
和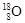 组成的水分子的物质的量 mol,其中含中子数为 mol,电子数为 个。
组成的水分子的物质的量 mol,其中含中子数为 mol,电子数为 个。
②请画出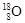 2-微粒的结构示意图: 。
2-微粒的结构示意图: 。
(2)质量相等的两种物质SO2和SO3,两种物质中硫元素质量之比为 ,分子物质的量之比为 ,所含氧原子个数之比为 。
(3)0.2L 0.5mol/L Al2(SO4)3溶液和0.5L 0.5mol/L Al2(SO4)3溶液所含SO42—离子浓度之比为____________,SO42—离子数目之比为____________。
(4)20.6g NaR 含有Na+0.2mol,则NaR的摩尔质量为 ,则含R 8.0g 的NaR的物质的量为 mol 。
(5)实验室用二氧化锰与浓盐酸反应制取氯气,反应方程式如下:
MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑。若0.1 molMnO4与足量的浓盐酸充分反应,则有 mol HCl被氧化,转移电子的物质的量为 mol,产生的Cl 2在标准状况下的体积为 L。
MnCl2+2H2O+Cl2↑。若0.1 molMnO4与足量的浓盐酸充分反应,则有 mol HCl被氧化,转移电子的物质的量为 mol,产生的Cl 2在标准状况下的体积为 L。
(1)①0.5 6 5NA ②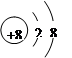
(2)5:4 5:4 5:6 (3)1:1 2:5 (4)103g/mol 0.1 (5)0.2 0.2 2.24
解析试题分析:(1)①由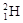 和
和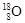 组成的水分子的摩尔质量是22g/mol,所以11g由
组成的水分子的摩尔质量是22g/mol,所以11g由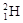 和
和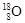 组成的水分子的物质的量=11g÷22g/mol=0.5mol。又因为质子数+中子数=质量数,所以其中含中子数为[(2-1)×2+18-8]×0.5mol=6mol。由于质子数=核外电子数,所以电子数为(1×2+8)×0.5×NA=5NA 个。
组成的水分子的物质的量=11g÷22g/mol=0.5mol。又因为质子数+中子数=质量数,所以其中含中子数为[(2-1)×2+18-8]×0.5mol=6mol。由于质子数=核外电子数,所以电子数为(1×2+8)×0.5×NA=5NA 个。
②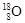 2-微粒的核外电子数是8+2=10个,所以该微粒的结构示意图为
2-微粒的核外电子数是8+2=10个,所以该微粒的结构示意图为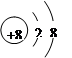 。
。
(2)质量相等的两种物质SO2和SO3,其物质的量之比=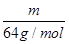 :
: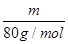 =5:4,所以两种物质中硫元素质量之比为5:4,分子物质的量之比为5:4,所含氧原子个数之比为2×5:3×4=5:6。
=5:4,所以两种物质中硫元素质量之比为5:4,分子物质的量之比为5:4,所含氧原子个数之比为2×5:3×4=5:6。
(3)0.2L 0.5mol/L Al2(SO4)3溶液中SO42—离子浓度是0.5mol/L×3=1.5mol/L,0.5L 0.5mol/L Al2(SO4)3溶液中SO42—离子浓度=0.5mol/L×3=1.5mol/L,因此所含SO42—离子浓度之比为1:1,SO42—离子数目之比为0.2L×1.5mol/L:0.5L×1.5mol/L=2:5。
(4)20.6g NaR 含有Na+0.2mol,则NaR的物质的量也是0.2mol,则其摩尔质量为20.6g÷0.2mol=103g/mol。这说明R的相对原子质量是103-23=80,则8.0gR的物质的量=8.0g÷80g/mol=0.1mol,所以含R 8.0g 的NaR的物质的量也是0.1mol 。
(5)根据反应MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑可知,镁消耗1mol二氧化锰的同时消耗4mol氯化氢,生成1mol氯气,这说明被氧化的氯化氢是2mol,所以若0.1 molMnO4与足量的浓盐酸充分反应,则有0.2mol HCl被氧化。锰元素的化合价从+4价降低到+2价,因此转移电子的物质的量为(4-2)×0.1mol=0.2mol,氯气的物质的量是0.1mol,则产生的Cl 2在标准状况下的体积为 0.1mol×22.4L/mol=2.24L。
MnCl2+2H2O+Cl2↑可知,镁消耗1mol二氧化锰的同时消耗4mol氯化氢,生成1mol氯气,这说明被氧化的氯化氢是2mol,所以若0.1 molMnO4与足量的浓盐酸充分反应,则有0.2mol HCl被氧化。锰元素的化合价从+4价降低到+2价,因此转移电子的物质的量为(4-2)×0.1mol=0.2mol,氯气的物质的量是0.1mol,则产生的Cl 2在标准状况下的体积为 0.1mol×22.4L/mol=2.24L。
考点:考查物质的量、物质的量浓度以及氧化还原反应的有关计算以及微粒结构示意图的书写

(10分)按要求填空:
(1)以下物质:①NH3 ②CaCO3 ③酒精 ④饱和食盐水 ⑤Cu ⑥KOH ⑦HCl属于电解质的有 (填编号);
(2)14.7gH2SO4分子所含氢原子数与 L (标准状况下)NH3所含氢原子数相等;
(3)固体NaCl(I2)(括号内的物质为杂质),除去杂质的方法为 。
(4)要除去某食盐晶体中的CaCl2、MgCl2、Na2SO4等杂质,有以下操作:
| A.蒸发结晶 | B.过滤 | C.加入过量的Na2CO3溶液 | D.加水溶解 E、加入过量的烧碱溶液 F、加入过量稀盐酸 G、加入过量的Ba(NO3)2溶液 H、加入过量的稀硝酸 I、加入过量的BaCl2溶液 |
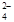 + 2Fe2+ + 4H+
+ 2Fe2+ + 4H+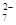 + 6 Fe2+ + 14 H+ →2 Cr3+ + 6 Fe3+ + 7 H2O
+ 6 Fe2+ + 14 H+ →2 Cr3+ + 6 Fe3+ + 7 H2O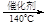 4N2 + 6H2O 6NO2 + 8NH3
4N2 + 6H2O 6NO2 + 8NH3