题目内容
19.白酒、食醋、淀粉、蔗糖等均为家庭厨房中利用这些物质能完成下列实验的是( )①检验自来水中是否含氯离子②鉴别食盐和小苏打③蛋壳能否溶于酸④无水乙醇中是否含有水.
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
分析 ①检验氯离子的存在通常用硝酸银;
②小苏打即为NaHCO3,能与醋酸反应生成二氧化碳气体;
③蛋壳中含有的碳酸钙,能与醋酸反应生成二氧化碳气体;
④一般用无水硫酸铜检验水.
解答 解:①检验氯离子的存在通常用硝酸银,通过是否生成白色沉淀来判断,故用所给的试剂无法实现,故①错误;
②小苏打即为NaHCO3,能与醋酸反应生成二氧化碳气体,而食盐不能,故可以用食醋来鉴别,故②正确;
③蛋壳中含有的碳酸钙,能与醋酸反应生成二氧化碳气体,故可以用食醋来验证,故③正确;
④一般用无水硫酸铜检验水,白酒、食醋、淀粉、蔗糖都不能检验水,故④错误.
故选C.
点评 本题考查物质检验及鉴别,题目难度不大,本题注意相关基础知识的积累,楚常见物质的主要成分,熟练掌握常见离子的检验.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
9. 盐酸、醋酸和碳酸是化学实验和研究中常用的几种酸.
盐酸、醋酸和碳酸是化学实验和研究中常用的几种酸.
已知室温下:Ka(CH3COOH)=1.7×10-5 mol•L-1;H2CO3的电离常数Ka1=4.2×10-7mol•L-1、Ka2=5.6×10-11mol•L-1
(1)常温下,物质的量浓度相同的下列四种溶液:a、氢氧化钡溶液b、氢氧化钠溶液c、碳酸钠溶液d、碳酸氢钠溶液e、醋酸钠溶液.其PH由大到小的顺序是:a>b>c>d>e(填序号).
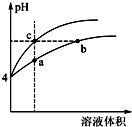
(2)某温度下,pH均为4的盐酸和醋酸溶液分别加水稀释,其pH随溶液体积变化的曲线图中a、b、c三点对应的溶液中水的电离程度由大到小的顺序是b=c>a;该醋酸溶液稀释过程中,下列各量一定变小的是ad.
a.c(H+) b.c(OH-) c.$\frac{c(C{H}_{3}COOH)c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})}$ d.$\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$
(3)以0.10mol•L-1NaOH为标准液,测定某盐酸的浓度.取20.00mL待测盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用NaOH标准溶液进行滴定.重复上述滴定操作2~3次,记录数据如下.
①滴定达到终点的标志是最后一滴NaOH溶液加入,溶液由无色恰好变成浅红色且半分钟内不褪色.
②根据上述数据,可计算出该盐酸的浓度约为0.12mol/L.
(4)在t℃时,某NaOH稀溶液中c(H+)=10-a mol•L-1,c(OH-)=10-b mol•L-1,已知a+b=12,则:
①该温度下水的离子积常数Kw=10-12mol2•L-2.
②在该温度下,将100mL0.1mol•L-1的稀H2SO4与100mL0.4mol•L-1的NaOH溶液混合后,溶液的pH=11.
 盐酸、醋酸和碳酸是化学实验和研究中常用的几种酸.
盐酸、醋酸和碳酸是化学实验和研究中常用的几种酸.已知室温下:Ka(CH3COOH)=1.7×10-5 mol•L-1;H2CO3的电离常数Ka1=4.2×10-7mol•L-1、Ka2=5.6×10-11mol•L-1
(1)常温下,物质的量浓度相同的下列四种溶液:a、氢氧化钡溶液b、氢氧化钠溶液c、碳酸钠溶液d、碳酸氢钠溶液e、醋酸钠溶液.其PH由大到小的顺序是:a>b>c>d>e(填序号).
(2)某温度下,pH均为4的盐酸和醋酸溶液分别加水稀释,其pH随溶液体积变化的曲线图中a、b、c三点对应的溶液中水的电离程度由大到小的顺序是b=c>a;该醋酸溶液稀释过程中,下列各量一定变小的是ad.
a.c(H+) b.c(OH-) c.$\frac{c(C{H}_{3}COOH)c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})}$ d.$\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$
(3)以0.10mol•L-1NaOH为标准液,测定某盐酸的浓度.取20.00mL待测盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用NaOH标准溶液进行滴定.重复上述滴定操作2~3次,记录数据如下.
| 实验编号 | 氢氧化钠溶液的浓度(mol•L-1) | 滴定完成时,氢氧化钠溶液滴入的体积(mL) | 待测盐酸的体积(mL) |
| 1 | 0.10 | 24.12 | 20.00 |
| 2 | 0.10 | 23.88 | 20.00 |
| 3 | 0.10 | 24.00 | 20.00 |
②根据上述数据,可计算出该盐酸的浓度约为0.12mol/L.
(4)在t℃时,某NaOH稀溶液中c(H+)=10-a mol•L-1,c(OH-)=10-b mol•L-1,已知a+b=12,则:
①该温度下水的离子积常数Kw=10-12mol2•L-2.
②在该温度下,将100mL0.1mol•L-1的稀H2SO4与100mL0.4mol•L-1的NaOH溶液混合后,溶液的pH=11.
10.(共4分)铬酸根CrO42-呈黄色,重铬酸根Cr2O72-呈橙色.在水溶液中,铬酸根离子和重铬酸根离子存在下列平衡:Cr2O72-+H2O?2CrO42-+2H+.在两支试管中分别取重铬酸钾溶液进行下列实验,完成下列表格.
| 试管1:滴加3滴浓硫酸 | 试管2:滴加3滴NaOH溶液 | |
| 实验现象 | ||
| 实验结论 |
7.根据下列性质判断所描述的物质可能属于分子晶体的是( )
| A. | 熔点1070℃,易溶于水,水溶液能导电 | |
| B. | 熔点1128℃,沸点4446℃,硬度很大 | |
| C. | 熔点10.31℃,液态不导电,水溶液能导电 | |
| D. | 熔点97.81℃,质软,导电,密度0.97g/cm3 |
4.锂~碘电池可用来为心脏起搏器提供能源,其电池反应可表示为:2Li+I2→2LiI.下列有关说法错误的是( )
| A. | 放电时化学能转化为电能 | B. | 负极反应为:Li-e=Li+ | ||
| C. | 正极反应为:I2+2e-=2I- | D. | 电流由负极流向正极 |
8.下列有关物质性质的说法错误的是( )
| A. | 热稳定性:HCl>HI | B. | 原子半径:Na>Mg | ||
| C. | 结合质子能力:S2->Cl- | D. | 酸性:H2SO3>H2SO4 |
9.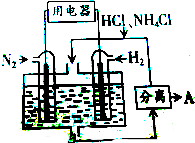 如图所示使用新型电极材料 以N2、H2 为电极反应物,以HCl-NH4Cl为电解质溶液组成的既能提供能量又能实现氮固定的新型电池.下列说法正确的是( )
如图所示使用新型电极材料 以N2、H2 为电极反应物,以HCl-NH4Cl为电解质溶液组成的既能提供能量又能实现氮固定的新型电池.下列说法正确的是( )
 如图所示使用新型电极材料 以N2、H2 为电极反应物,以HCl-NH4Cl为电解质溶液组成的既能提供能量又能实现氮固定的新型电池.下列说法正确的是( )
如图所示使用新型电极材料 以N2、H2 为电极反应物,以HCl-NH4Cl为电解质溶液组成的既能提供能量又能实现氮固定的新型电池.下列说法正确的是( )| A. | 通氮气的一极为负极 | |
| B. | 通氢气的一极发生还原反应 | |
| C. | 该电池的正极反应式为:N2+6e-+8H+═2NH4+ | |
| D. | 生产中可分离出的物质A的化学式为NH3 |