题目内容
8.下列有关物质性质的说法错误的是( )| A. | 热稳定性:HCl>HI | B. | 原子半径:Na>Mg | ||
| C. | 结合质子能力:S2->Cl- | D. | 酸性:H2SO3>H2SO4 |
分析 A.元素的非金属性越强,对应的氢化物越稳定;
B.同周期元素从左到右原子半径逐渐减小;
C.酸越弱,对应的阴离子越易结合质子;
D.元素的化合价越高,对应的含氧酸的酸性越强.
解答 解:A.非金属性:Cl>I,元素的非金属性越强,对应的氢化物越稳定,故A正确;
B.同周期元素从左到右原子半径逐渐减小,则原子半径:Na>Mg,故B正确;
C.酸性HCl>H2S,酸越弱,对应的阴离子越易结合质子,故C正确;
D.元素的化合价越高,对应的含氧酸的酸性越强,故D错误.
故选D.
点评 本题综合考查元素周期律知识,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
18.下列互为同位素的一组是( )
| A. | 氕、氘、氚 | B. | 白磷、红磷 | C. | 金刚石、石墨、C60 | D. | O2、O3 |
3.如图是高温下某反应的微观过程.下列说法中正确的是( )
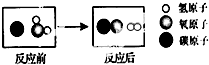

| A. | 该反应属于复分解反应 | B. | 该反应中元素的化合价没有变化 | ||
| C. | 图中的两种化合物都属于氧化物 | D. | 该反应所得生成物的质量比为1:1 |
13.X、Y、Z、W为四种短周期主族元素.其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6.下列说法正确的是( )
| A. | Y、Z两元素的简单离子的半径Y>Z | |
| B. | Y元素最高价氧化物对应水化物的化学式为H2YO4 | |
| C. | 原子序数由小到大的顺序为W<X<Y<Z | |
| D. | X与W可以形成W2X、W2X2两种化合物 |
20.下列各组元素中,按最高正化合价递增顺序排列的是( )
| A. | C、N、F | B. | Na、Mg、Al | C. | F、Cl、Br | D. | Cl、S、P |
18. 如图是铅蓄电池充、放电时的工作示意图,电解质是H2SO4溶液.已知放电时电池反应为:Pb+PbO2+4H++2SO42-═2PbSO4+2H2O.下列有关说法正确的是( )
如图是铅蓄电池充、放电时的工作示意图,电解质是H2SO4溶液.已知放电时电池反应为:Pb+PbO2+4H++2SO42-═2PbSO4+2H2O.下列有关说法正确的是( )
 如图是铅蓄电池充、放电时的工作示意图,电解质是H2SO4溶液.已知放电时电池反应为:Pb+PbO2+4H++2SO42-═2PbSO4+2H2O.下列有关说法正确的是( )
如图是铅蓄电池充、放电时的工作示意图,电解质是H2SO4溶液.已知放电时电池反应为:Pb+PbO2+4H++2SO42-═2PbSO4+2H2O.下列有关说法正确的是( )| A. | K与N相接时,能量由电能转化为化学能 | |
| B. | K与N相接时,Pb上发生反应为:Pb-2e-═Pb2+ | |
| C. | K与M连接时,所用电源的a极为负极 | |
| D. | K与M连接时,PbO2上发生反应为:PbO2+4e_+4H++SO42-═PbSO4+2H2O |
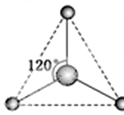 有一种活性反应中间体微粒,它的微粒中含有1个碳原子和3个氢原子.请依据下面给出的这种微粒的球棍模型,写出相应的化学式:CH3+.
有一种活性反应中间体微粒,它的微粒中含有1个碳原子和3个氢原子.请依据下面给出的这种微粒的球棍模型,写出相应的化学式:CH3+.