题目内容
17.阿司匹林(H)是常用的解热镇痛药物,可由下列流程合成阿司匹林(H)和一种高聚物(G):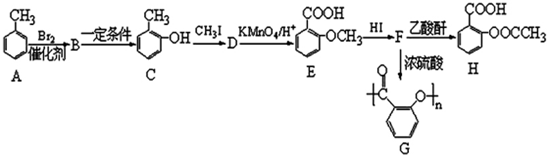
(1)B的结构简式是
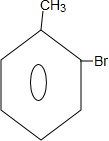 ;B→C的反应类型是取代反应.
;B→C的反应类型是取代反应.(2)C名称是邻甲基苯酚;H中含氧官能团的名称是羧基和酯基.
(3)由F合成高聚物G的化学方程式是n
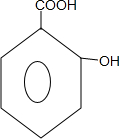 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$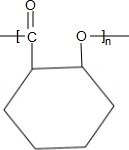 +nH2O.
+nH2O.(4)E有多种同分异构体.写出符合下列条件E的同分异构体的结构简式:
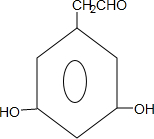 、
、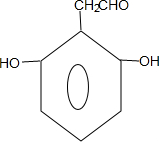 .
.①含有醛基且不能发生水解反应;
②能与FeCl3溶液发生显色反应,且1mol 该物质能与2mol NaOH反应;
③分子中核磁共振氢谱显示有五组峰
(5)下列说法正确的是abc(填字母序号).
a.A使溴水褪色是物理变化
b.C不能与NaHCO3溶液发生反应
c.E可与乙醇在一定条件下发生取代反应
d.1mol H与足量NaOH溶液反应,最多消耗2mol NaOH.
分析 通过合成阿司匹林的流程图,结合反应条件可知,甲苯与溴发生取代反应生成的B为 ,B发生取代反应生成C,C为邻甲基苯酚,为保护酚羟基,防止用酸性高锰酸钾氧化甲基时氧化掉,设计了C→D,E→F两步,F为邻羟基苯甲酸,结构简式为
,B发生取代反应生成C,C为邻甲基苯酚,为保护酚羟基,防止用酸性高锰酸钾氧化甲基时氧化掉,设计了C→D,E→F两步,F为邻羟基苯甲酸,结构简式为 ,F通过缩聚反应生成高聚物G,通过取代反应生成阿司匹林,据此分析.
,F通过缩聚反应生成高聚物G,通过取代反应生成阿司匹林,据此分析.
解答 解:(1)通过合成阿司匹林的流程图,结合反应条件可知,甲苯与溴发生取代反应生成的B为 ,B发生取代反应生成C,
,B发生取代反应生成C,
故答案为: ;取代反应;
;取代反应;
(2)C为邻甲基苯酚,据H的结构简式可知,H中含有羧基和酯基两种官能团,故答案为:邻甲基苯酚;羧基和酯基;
(3)F为邻羟基苯甲酸,结构简式为 ,F通过缩聚反应生成高聚物G,化学方程式为n
,F通过缩聚反应生成高聚物G,化学方程式为n $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +nH2O,故答案为:n
+nH2O,故答案为:n $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +nH2O;
+nH2O;
(4)E中除苯环外还有2个C原子和3个O原子,①含有醛基且不能发生水解反应,说明含义醛基且不是甲酸酯基;
②能与FeCl3溶液发生显色反应,且1mol 该物质能与2mol NaOH反应,说明含义2个酚羟基;
③分子中核磁共振氢谱显示有五组峰,说明酚羟基对称,苯环上有2种氢原子,其结构简式为 ,
, ,
,
故答案为: ;
; ;
;
(5)a.A不能和溴水反应,可以萃取溴,所以A使溴水褪色是物理变化,故a正确;
b.C中有酚羟基,不能与NaHCO3溶液发生反应,故b正确;
c.E中有羧基,可与乙醇在一定条件下发生取代反应,故c正确;
d.1molH在NaOH溶液中水解,生成2mol羧基、1mol酚羟基,都能与NaOH反应,所以1mol H与足量NaOH溶液反应,最多消耗3mol NaOH,故d错误;
故答案为:abc.
点评 本题考查有机物的合成,题目难度不大,本题注意把握常见有机物的官能团的性质,记住反应条件,常见有机物反应的化学方程式要会写.

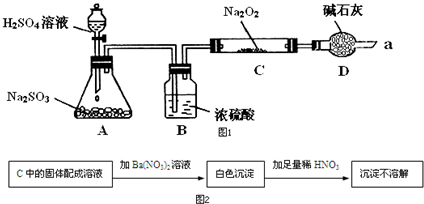 某同学想通过如图装置实验、探究SO2与Na2O2反应的产物.(夹持装置已略去,装置的气密性良好)
某同学想通过如图装置实验、探究SO2与Na2O2反应的产物.(夹持装置已略去,装置的气密性良好)Ⅰ.装置B的作用是吸收水,干燥SO2气体,其原因是(用离子方程式表示)2Na2O2+2H2O=4Na++4OH-+O2↑.装置D除了吸收过量的SO2,避免污染空气外,还起到的作用是防止空气中的水蒸气和二氧化碳进入C装置与Na2O2反应.
Ⅱ.某同学想通过图2实验装置,检验反应中是否有O2生成时,其实验操作步骤是:
①先打开分液漏斗上口瓶塞和下口旋塞
②再用带火星的木条靠近干燥管口a,观察其是否复燃.
Ⅲ.对C中固体产物提出如下假设:
假设1:只有Na2SO3
假设2:只有Na2SO4
假设3:有Na2SO3和Na2SO4.
(1)若假设2成立,写出所发生反应的化学方程式Na2O2+SO2=Na2SO4.
(2)若Na2O2反应完全,为确定C中固体产物的成分,甲设计如图2实验,C中的固体配成溶液加Ba(NO3)2溶液沉淀不溶解白色沉淀加足量稀HNO3.
得出结论:产物是Na2SO4.
该方案是否合理否 (填“是”或“否”).
(3)设计实验验证假设3的实验步骤如表:
| 实验步骤 | 实验现象 |
| ①滴加入过量的稀盐酸 | 产生剌激性气味气体 |
| ②滴加入适量的BaCl2溶液 | 产生白色沉淀. |
| ③取少量C中固体产物于试管中,加入适量的蒸馏水溶解 |
| 元素代号 | A | B | C | D | E | F | G | H |
| 化合价 | -1 | -2 | +4、-4 | +7、-1 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
| A. | A的单质能从GD2溶液中置换出D单质 | |
| B. | G在CB2中燃烧生成两种化合物 | |
| C. | E元素的单质不存在同素异形体 | |
| D. | A、F、H的离子半径由大到小顺序是A>H>F |
| A. | 1 mo1 Na2O2与足量H2O反应,转移了2 NA 个电子 | |
| B. | 1 mol O2在反应中得到电子数一定为4 NA | |
| C. | 1 mol Cl2在反应中得到电子数不一定为2NA | |
| D. | 在2KClO3+4HC1(浓)═2KCl+2C1O2↑+C12↑+2H2O中,氯气既是氧化产物又是还原产物,每生成1 mol Cl2转移2 NA 个电子 |
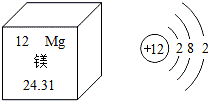
| A. | 镁原子的核电荷数为12 | |
| B. | 镁原子的相对原子质量为24.31g | |
| C. | 镁属于非金属元素 | |
| D. | 在化学反应中,镁原子容易得到电子 |
| A. | Cl- | B. | F - | C. | S2- | D. | Br |
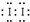 (用电子式表示).
(用电子式表示).