题目内容
5.几种短周期元素的原子半径及某些化合价见下表,下列说法正确的是( )| 元素代号 | A | B | C | D | E | F | G | H |
| 化合价 | -1 | -2 | +4、-4 | +7、-1 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
| A. | A的单质能从GD2溶液中置换出D单质 | |
| B. | G在CB2中燃烧生成两种化合物 | |
| C. | E元素的单质不存在同素异形体 | |
| D. | A、F、H的离子半径由大到小顺序是A>H>F |
分析 A、D的化合价都有-1,且D的原子半径较大,还有+7价,则A为F元素、D为Cl;B的化合价为-2,原子半径小于Cl,故B为O元素;C的化合价为+4、-4,原子半径小于Cl,故C为碳元素;E的化合价为+5、-3,原子半径大于Cl,故E为P元素;F、G的化合价分别为+3、+2,原子半径都大于P,故F为Al、G为Mg,H的化合价为+1,原子半径大于Mg,故H为Na,据此进行解答.
解答 解:A、D的化合价都有-1,且D的原子半径较大,还有+7价,则A为F元素、D为Cl;B的化合价为-2,原子半径小于Cl,故B为O元素;C的化合价为+4、-4,原子半径小于Cl,故C为碳元素;E的化合价为+5、-3,原子半径大于Cl,故E为P元素;F、G的化合价分别为+3、+2,原子半径都大于P,故F为Al、G为Mg,H的化合价为+1,原子半径大于Mg,故H为Na,
A.氟气与水反应生成HF与氧气,不能将氯气从氯化镁溶液中置换出来,故A错误;
B.Mg在二氧化碳中燃烧生成MgO与碳,故B错误;
C.磷的单质存在红磷、白磷同素异形体,故C错误;
D.电子层结构相同,核电荷数越大离子半径越小,故离子半径F->Na+>Al3+,故D正确,
故选D.
点评 本题考查结构性质位置关系应用,题目难度中等,根据化合价及原子半径推断元素是解题关键,注意对元素周期律的理解掌握,A选项为易错点,中学较少涉及氟气的有关性质.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
16.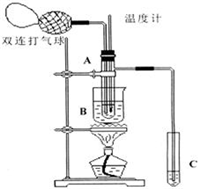 乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见下表:
乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见下表:
请回答下列问题:
(1)试管A内在60~80℃时发生的主要反应的化学方程式为(注明反应条件)2CH3CHO+O2$→_{CuO}^{60℃-80℃}$2CH3COOH;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在试管A的反应液中;目的是测量反应溶液的温度;当试管A内的主要反应完成后温度计水银球的位置应在试管A的支管口处,目的是收集含乙酸的馏分;
(3)烧杯B的作用是使试管A内的反应液均匀受热发生反应,使生成的乙酸变成蒸气进入试管C;烧杯B内盛装的液体可以是乙二醇(甘油)(写出一种即可,在题给物质中找);
(4)若想检验试管C中是否含有产物乙酸,请你在所提供的药品中进行选择,设计一个简便的实验方案.所提供的药品有:pH试纸、红色的石蕊试纸、白色的醋酸铅试纸、碳酸氢钠粉末.实验仪器任选.该方案为:
将少量碳酸氢钠粉未,放入一个洁净的试管中,加入少量试管C中的液体,若有气体产生,则说明试管C中含有产物乙酸(或把一块pH试纸放在表面皿(或玻璃片)上,用洁净、干燥的玻璃棒蘸取试管C内的液体,点在pH试纸中部,试纸变色后,用标准比色卡比较来确定溶液的pH,进而说明是否有乙酸生成).
 乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见下表:
乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见下表:| 物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
| 沸点 | 20.8℃ | 117.9℃ | 290℃ | 197.2℃ | 100℃ |
(1)试管A内在60~80℃时发生的主要反应的化学方程式为(注明反应条件)2CH3CHO+O2$→_{CuO}^{60℃-80℃}$2CH3COOH;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在试管A的反应液中;目的是测量反应溶液的温度;当试管A内的主要反应完成后温度计水银球的位置应在试管A的支管口处,目的是收集含乙酸的馏分;
(3)烧杯B的作用是使试管A内的反应液均匀受热发生反应,使生成的乙酸变成蒸气进入试管C;烧杯B内盛装的液体可以是乙二醇(甘油)(写出一种即可,在题给物质中找);
(4)若想检验试管C中是否含有产物乙酸,请你在所提供的药品中进行选择,设计一个简便的实验方案.所提供的药品有:pH试纸、红色的石蕊试纸、白色的醋酸铅试纸、碳酸氢钠粉末.实验仪器任选.该方案为:
将少量碳酸氢钠粉未,放入一个洁净的试管中,加入少量试管C中的液体,若有气体产生,则说明试管C中含有产物乙酸(或把一块pH试纸放在表面皿(或玻璃片)上,用洁净、干燥的玻璃棒蘸取试管C内的液体,点在pH试纸中部,试纸变色后,用标准比色卡比较来确定溶液的pH,进而说明是否有乙酸生成).
13.下列说法不正确的是( )
| A. | 某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性 | |
| B. | 在稀硫酸中加入铜粉,铜粉不溶解,再加入Cu(NO3)2固体,铜粉仍不溶解 | |
| C. | 铜与稀硝酸反应的离子方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| D. | HNO3→NO→NO2,以上各步变化均能通过一步实现 |
20.在透明溶液中能大量共存的是( )
| A. | K+、Cu2+、Na+、Cl- | B. | H+、Na+、NO3-、HCO3- | ||
| C. | Ba2+、H+、NO3-、SO42- | D. | Mg2+、Na+、OH-、SO42- |
10.化学与生产、生活密切相关,下列说法不正确的是( )
| A. | 84消毒液(主要成分NaClO)与洁厕剂混合使用可能会导致中毒 | |
| B. | 晶体硅可用于光伏发电、制造芯片,硅酸钠可用于制备硅胶和木材防火剂;硅胶可用作袋装食品的干燥剂 | |
| C. | 小苏打可中和胃酸、热纯碱可除去油污 | |
| D. | 二氧化硫可广泛用于食品的增白及漂白纸浆、毛、丝、草帽辫等 |
14.下列实验方法或操作正确的是( )
| A. |  转移溶液 | B. |  制蒸馏水 | C. |  分离水和酒精 | D. |  稀释浓硫酸 |
15.下列图示与对应的叙述不相符的是( )
| A. | 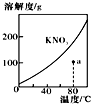 表示KNO3的溶解度曲线,a点所示的溶液是80℃时KNO3不饱和溶液 | |
| B. |  表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 | |
| C. |  表示0.1000mol/LNaOH滴定20.00 mL 0.1000mol/L醋酸的滴定曲线 | |
| D. | 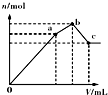 表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,体积V与沉淀n的变化 |
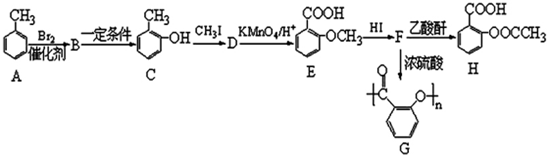
 合成
合成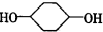 (部分试剂和反应条件已去).请回答下列问题:
(部分试剂和反应条件已去).请回答下列问题:
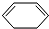 +Br$\stackrel{一定条件}{→}$
+Br$\stackrel{一定条件}{→}$ ,写出在同样条件下CH2=CH-CH=CH2与等物质的量Br发生加成反应的化学方程式:
,写出在同样条件下CH2=CH-CH=CH2与等物质的量Br发生加成反应的化学方程式: .
. F
F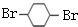 .
. ,其PMR谱中有2个信号峰,其强度之比为3:1.则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1:1:2的是BD.
,其PMR谱中有2个信号峰,其强度之比为3:1.则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1:1:2的是BD.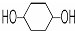 B.
B.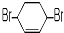 C.
C. D.
D.
 的化学方程式(有机物写结构简式,注明反应条件)
的化学方程式(有机物写结构简式,注明反应条件) .
.
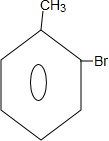 ;B→C的反应类型是取代反应.
;B→C的反应类型是取代反应.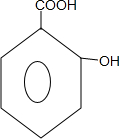 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$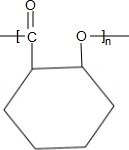 +nH2O.
+nH2O.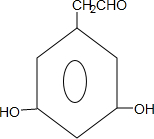 、
、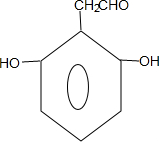 .
.