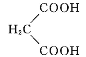题目内容
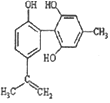
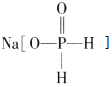
【题目】![]() 和
和![]() 能发生反应
能发生反应![]() 未配平
未配平![]() :
:![]() 。该反应的速率v随
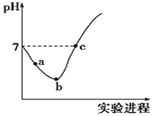
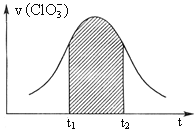
。该反应的速率v随![]() 的增大而增大,如图是v
的增大而增大,如图是v ![]() 图。下列说法中不正确的是
图。下列说法中不正确的是
A.开始时反应速率增大可能是由![]() 增大所致
增大所致
B.纵坐标为![]() 的
的![]() 曲线与图曲线完全重合
曲线与图曲线完全重合
C.后期反应速率下降的主要原因是反应物浓度减小
D.阴影部分面积可以表示![]() 时间内
时间内![]() 增加
增加
【答案】B
【解析】
A.由题目信息可知反应的速率随![]() 的增大而加快;
的增大而加快;
B.先根据电子得失守恒和原子守恒配平方程式,然后根据速率之比等于化学计量数之比;
C.根据随着反应的进行,反应物的浓度减少,反应速率减小;
D.先根据电子得失守恒和原子守恒配平方程式,然后根据改变的物质的量之比等于化学计量数之比判断。
A.由方程式![]() 可知:反应开始时随着反应的进行,
可知:反应开始时随着反应的进行,![]() 不断增大,反应的速率加快,由题目信息可知反应的速率随
不断增大,反应的速率加快,由题目信息可知反应的速率随![]() 的增大而加快,故A正确;
的增大而加快,故A正确;
B.在反应![]() 中,
中,![]() 参加氧化还原反应得到6mol电子,1mol亚硫酸氢根离子参加氧化还原反应失去2mol电子,所以得失电子的最小公倍数是6,则
参加氧化还原反应得到6mol电子,1mol亚硫酸氢根离子参加氧化还原反应失去2mol电子,所以得失电子的最小公倍数是6,则![]() 的计量数是1,亚硫酸氢根离子的计量数是3,其它原子根据原子守恒来配平,所以该方程式为:
的计量数是1,亚硫酸氢根离子的计量数是3,其它原子根据原子守恒来配平,所以该方程式为:![]() ,
,![]() :
:![]() :3,纵坐标为
:3,纵坐标为![]() 的
的![]() 曲线与图中曲线不重合,故B错误;
曲线与图中曲线不重合,故B错误;
C.随着反应的进行,反应物的浓度减少,反应速率减小,所以后期反应速率下降的主要原因是反应物浓度减小,故C正确;
D.配平的化学方程式为:![]() ,
,![]() :
:![]() :1,所以图中阴影部分面积可以表示
:1,所以图中阴影部分面积可以表示![]() 时间为
时间为![]() 增加,故D正确;
增加,故D正确;
答案:B。

练习册系列答案
相关题目