题目内容
下列盐溶液能发生水解的用离子方程式表示,不能发生水解的写“不发生水解”字样,并说明溶液的酸碱性:
K2CO3 ,溶液呈 性;
Na2SO4 ,溶液呈 性.
K2CO3
Na2SO4
考点:盐类水解的应用
专题:盐类的水解专题
分析:碳酸钾为强碱弱酸盐,碳酸根离子水解导致溶液呈碱性,硫酸钠为强碱强酸盐,不水解,溶液呈中性.
解答:
解:碳酸钾为强碱弱酸盐,碳酸根离子水解导致溶液呈碱性,水解方程式为CO32-+H2O?OH-+HCO3-,硫酸钠为强碱强酸盐,钠离子和硫酸根离子都不水解,溶液呈中性,
故答案为:CO32-+H2O?OH-+HCO3-;碱;不水解;中性.
故答案为:CO32-+H2O?OH-+HCO3-;碱;不水解;中性.
点评:本题考查了盐类水解,明确“谁强谁显性、谁弱谁水解、强强显中性”来分析解答即可,题目难度不大.

练习册系列答案
相关题目
在密闭容器中,加热等物质的量的NaHCO3和Na2O2的固体混合物,充分反应后,容器中固体剩余物是( )
| A、Na2CO3和Na2O2 |
| B、Na2CO3和NaOH |
| C、NaOH和Na2O2 |
| D、NaOH、Na2O2和Na2CO3 |
下列说法正确的是( )
| A、电解质与非电解质的本质区别是在水溶液或熔化状态下能否电离 |
| B、盐酸的导电性一定比醋酸的强 |
| C、酸、碱和盐类都属于电解质,其他化合物都是非电解质 |
| D、溶于水能导电的化合物一定是电解质 |
对实验A-D的实验现象预测正确的是( )
A、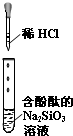 试管中红色溶液逐渐变成无色溶液 |
B、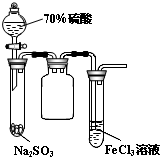 试管中出现淡黄色浑浊 |
C、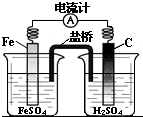 铁棒上有无色气泡产生 |
D、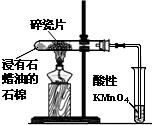 酸性KMnO4溶液中出现气泡且颜色逐渐褪去 |