题目内容
【题目】对于反应![]() 。采取下列措施能加快反应速率的是( )
。采取下列措施能加快反应速率的是( )
①升温 ②恒容下通入惰性气体 ③增加![]() 的浓度 ④减压 ⑤加催化剂 ⑥恒压下通入惰性气体
的浓度 ④减压 ⑤加催化剂 ⑥恒压下通入惰性气体
A.①②⑤B.①③⑤C.②④⑥D.③⑤⑥
【答案】B
【解析】
①升温,活化分子百分数增大,单位体积活化分子数目增多,反应速率加快,故①正确;
②恒容下通入惰性气体,反应体系中各物质的浓度不变,反应速率不变,故②错误;
③增加![]() 浓度,单位体积活化分子数目增多,反应速率增大,故③正确;
浓度,单位体积活化分子数目增多,反应速率增大,故③正确;
④减压,单位体积活化分子数目减小,反应速率减小,故④错误;
⑤加催化剂,可增大活化分子百分数,单位体积活化分子数目增多,反应速率增大,故⑤正确;
⑥恒压通入惰性气体,气体的体积增大,单位体积活化分子数目减小,反应速率减小,故⑥错误;
能加快反应速率的有①③⑤,故选B。

 阅读快车系列答案
阅读快车系列答案【题目】水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题:
(1)纯水在100 ℃时,pH=6,该温度下0.1 mol·L-1的NaOH溶液的pH=_____________。
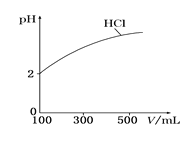
(2)体积均为100 mL、pH均为2的盐酸与一元弱酸HX,加水稀释过程中盐酸的pH与溶液体积的关系如图所示,则在图上画出HX加水至500mL稀释过程中pH值的变化曲线_____,并说明理由___________。
(3)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
化学式 | 电离平衡常数(25 ℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7,K2=5.6×10-11 |
25 ℃时,在0.5 mol·L-1的醋酸溶液中由醋酸电离出的c(H+)约是由水电离出的c(H+)的_____倍。
(4)写出在NaCN溶液中通入少量CO2反应的离子方程式________________________。
(5)某兴趣小组为研究碳酸钠水解平衡与温度的关系,用数字实验系统测定一定浓度碳酸钠溶液的pH与温度的关系,得到曲线如图,下列分析合理的是___________。
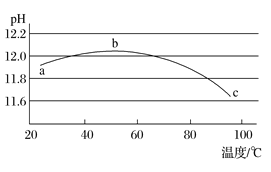
A 碳酸钠水解是吸热反应 B ab段说明水解平衡向右移动
C bc段说明水解平衡向左移动 D 水的电离平衡也对pH产生影响