题目内容
用NA表示阿伏德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4L SO3中含有的分子数为NA |
| B、2L 0.5mol/L的CH3COOH溶液中,含有CH3COO-离子个数为NA |
| C、常温常压下,3.4g NH3含有原子的数目为0.8NA个 |
| D、78g Na2O2与足量水反应转移的电子数目为2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.标准状况下,三氧化硫的状态不是气体,不能使用标况下的气体摩尔体积计算其物质的量;
B.乙酸为弱电解质,溶液中只能部分电离出醋酸根离子;
C.氨气分子中含有4个原子,3.4g氨气的物质的量为:
=0.2mol,含有0.8mol原子;
D.过氧化钠中氧元素化合价为-1价,根据过氧化钠与水完全反应生成氧气的物质的量计算出转移的电子数.
B.乙酸为弱电解质,溶液中只能部分电离出醋酸根离子;
C.氨气分子中含有4个原子,3.4g氨气的物质的量为:
| 3.4g |
| 17g/mol |
D.过氧化钠中氧元素化合价为-1价,根据过氧化钠与水完全反应生成氧气的物质的量计算出转移的电子数.
解答:
解:A.标况下,SO3不是气体,题中条件无法计算22.4LSO3的物质的量,故A错误;
B.2L 0.5mol/L的CH3COOH溶液中含有溶质醋酸的物质的量为:0.5mol/L×2L=1mol,1mol醋酸只能部分电离出醋酸根离子,所以溶液中醋酸根离子的物质的量小于1mol,CH3COO-离子个数小于NA,故B错误;
C.3.4g氨气的物质的量为:
=0.2mol,0.2molNH3含有0.8mol原子,含有原子的数目为0.8NA个,故C正确;
D.78g Na2O2的物质的量为:
=1mol,根据反应方程式2Na+2H2O=2Na++2OH-+H2↑可知,1mol过氧化钠与足量水反应生成0.5mol氧气,生成0.5mol氧气转移了1mol电子,转移的电子数目为NA,故D错误;
故选C.
B.2L 0.5mol/L的CH3COOH溶液中含有溶质醋酸的物质的量为:0.5mol/L×2L=1mol,1mol醋酸只能部分电离出醋酸根离子,所以溶液中醋酸根离子的物质的量小于1mol,CH3COO-离子个数小于NA,故B错误;
C.3.4g氨气的物质的量为:
| 3.4g |
| 17g/mol |
D.78g Na2O2的物质的量为:
| 78g |
| 78g/mol |
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标准状况下气体摩尔体积的使用条件,要求掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;选项B为易错点,注意醋酸为弱电解质,溶液中只能部分电离.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
用下列实验装置进行相应实验,能达到实验目的是( )
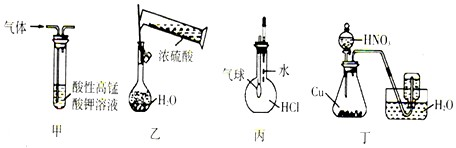

| A、装置甲:除去乙烯中混有的少量SO2 |
| B、装置乙:用浓硫酸配制1mol/L的硫酸 |
| C、装置丙:检验HCl气体在水中的溶解性 |
| D、装置丁:用铜和浓硝酸反应制取NO2 |
下列装置或操作能达到实验目的是( )
A、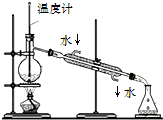 蒸馏石油 |
B、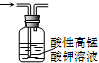 除去甲烷中少量乙烯 |
C、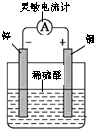 验证化学能转变电能 |
D、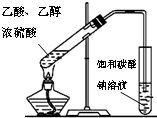 制取乙酸乙酯 |
“化学无处不在”,下列与化学有关的说法正确的是( )
| A、聚乙烯塑料的老化是因为发生了加成反应 |
| B、纤维素在人体内可水解为葡萄糖,故可作人类的营养物质 |
| C、合成纤维、人造纤维及碳纤维都属于有机高分子材料 |
| D、向某溶液中加入茚三酮试剂,加热煮沸后溶液若出现紫蓝色,则该溶液含有氨基酸 |
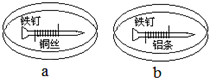 如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动),下列叙述正确的是( )
如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动),下列叙述正确的是( )| A、a中铁钉附近呈现红色 |
| B、b中铝条附近有气泡产生 |
| C、a中铜丝上发生氧化反应 |
| D、b中铁钉上发生还原反应 |
下列有关实验操作正确的是( )
| A、用Ba(NO3)2溶液可以鉴别SO32-和SO42- |
| B、做H2还原CuO实验时要先通氢气,验纯后再加热 |
C、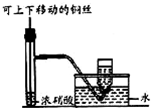 采用如图所示装置可制备并收集少量NO2气体 |
| D、测定相同温度下盐酸和醋酸溶液的pH,就可证明盐酸是强酸、醋酸是弱酸 |
下列物质中,可以用于制造半导体的是( )
| A、铝 | B、石墨 |
| C、晶体硅 | D、二氧化硅 |
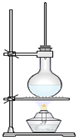 (1)在蔗糖中加入浓H2SO4,反应的化学方程式为
(1)在蔗糖中加入浓H2SO4,反应的化学方程式为