题目内容
下列装置或操作能达到实验目的是( )
A、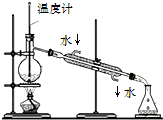 蒸馏石油 |
B、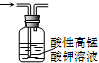 除去甲烷中少量乙烯 |
C、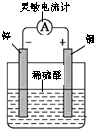 验证化学能转变电能 |
D、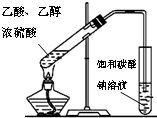 制取乙酸乙酯 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.温度计位置、冷却水的方向均不合理;
B.乙烯被高锰酸钾氧化后生成二氧化碳;
C.Zn比Cu活泼,形成原电池;
D.导管在碳酸钠溶液液面下,发生倒吸.
B.乙烯被高锰酸钾氧化后生成二氧化碳;
C.Zn比Cu活泼,形成原电池;
D.导管在碳酸钠溶液液面下,发生倒吸.
解答:
解:A.温度计测定馏分的温度,温度计的水银球应在烧瓶支管口处,冷却水的方向应为下进上出冷却效果好,故A错误;
B.乙烯被高锰酸钾氧化后生成二氧化碳,引入新杂质,应利用溴水来除杂,故B错误;
C.Zn比Cu活泼,形成原电池,发生Zn与硫酸的电池反应,将化学能转变为电能,故C正确;
D.导管在碳酸钠溶液液面下,发生倒吸,则导管应在碳酸钠溶液的液面以上,故D错误;
故选C.
B.乙烯被高锰酸钾氧化后生成二氧化碳,引入新杂质,应利用溴水来除杂,故B错误;
C.Zn比Cu活泼,形成原电池,发生Zn与硫酸的电池反应,将化学能转变为电能,故C正确;
D.导管在碳酸钠溶液液面下,发生倒吸,则导管应在碳酸钠溶液的液面以上,故D错误;
故选C.
点评:本题考查化学实验方案的评价,侧重于物质的检验、分离、制备及原电池等实验方案的评价,注意把握相关物质的性质,为解答该类题目的关键,题目难度不大.

练习册系列答案
 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案
相关题目
室温下,下列各组离子在指定溶液中能大量共存的是( )
| A、饱和氯水中:Cl-、NO3-、Na+、SO32- |
| B、pH=12的溶液中:NO3-、I-、Na+、ClO- |
| C、Na2S溶液中:SO42-、K+、Cl-、Cu2+ |
| D、c(H+)=1.0×10-13mol?L-1溶液中:CH3COO-、K+、SO42-、Br- |
一种氢镍电池的电极总反应是H2+2NiO(OH)═2Ni(OH)2,作为负极的是( )
| A、NiO(OH) |
| B、H2 |
| C、Ni |
| D、Ni(OH)2 |
用NA表示阿伏德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4L SO3中含有的分子数为NA |
| B、2L 0.5mol/L的CH3COOH溶液中,含有CH3COO-离子个数为NA |
| C、常温常压下,3.4g NH3含有原子的数目为0.8NA个 |
| D、78g Na2O2与足量水反应转移的电子数目为2NA |
反应 A+3B═2C+4D在不同情况下的反应速率最快的是( )
| A、υ(A)=0.4mol(L?s)-1 |
| B、υ(B)=0.8mol(L?s)-1 |
| C、υ(C)=0.6mol(L?s)-1 |
| D、υ(D)=1.0mol(L?s)-1 |
3.2g铜与过量硝酸(8mol?L-1,100mL)充分反应,硝酸的还原产物为NO2和NO,反应后溶液中含a mol H+,则此时溶液中所含NO3-的物质的量是( )
| A、0.2+a | B、0.1+a |
| C、0.05+a | D、a |
下列表述正确的是( )
| A、醛基的结构简式-COH |
| B、聚丙烯的结构简式[-CH2-CH2-CH2-]n |
C、四氯化碳分子的电子式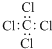 |
D、丙烷分子的球棍模型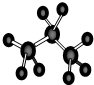 |