题目内容
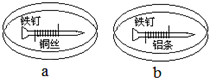 如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动),下列叙述正确的是( )
如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动),下列叙述正确的是( )| A、a中铁钉附近呈现红色 |
| B、b中铝条附近有气泡产生 |
| C、a中铜丝上发生氧化反应 |
| D、b中铁钉上发生还原反应 |
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:A.a中构成的是铁铜原电池,铁作为负极,发生氧化反应;
B.b中构成铁铝原电池,铝作负极,发生氧化反应;
C.a中构成的是铁铜原电池,铜作为正极,发生还原反应;
D.b中构成铁铝原电池,铝作负极,铁作正极,发生还原反应.
B.b中构成铁铝原电池,铝作负极,发生氧化反应;
C.a中构成的是铁铜原电池,铜作为正极,发生还原反应;
D.b中构成铁铝原电池,铝作负极,铁作正极,发生还原反应.
解答:
解:A.a中构成的是铁铜原电池,铁作为负极:Fe-2e-=Fe2+,发生氧化反应,没有红色出现,故A错误;
B.b中构成铁铝原电池,铝作负极:Al-3e-═Al3+,发生氧化反应,没有气泡产生,故B错误;
C.a中构成的是铁铜原电池,铜作为正极,发生还原反应,故C错误;
D.b中构成铁铝原电池,铝作负极,铁作正极,发生还原反应,故D正确;
故选D.
B.b中构成铁铝原电池,铝作负极:Al-3e-═Al3+,发生氧化反应,没有气泡产生,故B错误;
C.a中构成的是铁铜原电池,铜作为正极,发生还原反应,故C错误;
D.b中构成铁铝原电池,铝作负极,铁作正极,发生还原反应,故D正确;
故选D.
点评:本题考查原电池基础原理,难度不大,注意原电池两极判断与发生反应.

练习册系列答案
相关题目
用NA表示阿伏德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4L SO3中含有的分子数为NA |
| B、2L 0.5mol/L的CH3COOH溶液中,含有CH3COO-离子个数为NA |
| C、常温常压下,3.4g NH3含有原子的数目为0.8NA个 |
| D、78g Na2O2与足量水反应转移的电子数目为2NA |
反应 A+3B═2C+4D在不同情况下的反应速率最快的是( )
| A、υ(A)=0.4mol(L?s)-1 |
| B、υ(B)=0.8mol(L?s)-1 |
| C、υ(C)=0.6mol(L?s)-1 |
| D、υ(D)=1.0mol(L?s)-1 |
下列有关说法正确的是( )
| A、用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物 |
| B、镀锌铁板是利用了牺牲阳极的阴极保护法来达到防止腐蚀的目的 |
| C、取一定量水垢加盐酸,生成能使澄清石灰水变浑浊的气体,说明水垢的主要成分为CaCO3、MgCO3 |
| D、已知Cu2O+2H+═Cu2++Cu+H2O,氢气还原氧化铜后所得红色固体能完全溶于稀硝酸,说明还原产物是铜 |
3.2g铜与过量硝酸(8mol?L-1,100mL)充分反应,硝酸的还原产物为NO2和NO,反应后溶液中含a mol H+,则此时溶液中所含NO3-的物质的量是( )
| A、0.2+a | B、0.1+a |
| C、0.05+a | D、a |
既能与盐酸反应,又能与NaOH溶液反应的是( )
①Na2SiO3 ②Al(OH)3 ③NaHCO3 ④Al2O3.
①Na2SiO3 ②Al(OH)3 ③NaHCO3 ④Al2O3.
| A、①②④ | B、②③④ |
| C、②④ | D、全部 |