题目内容
用下列实验装置进行相应实验,能达到实验目的是( )
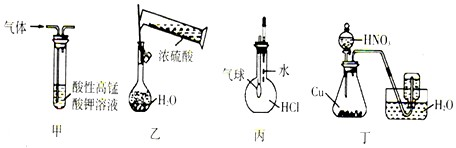

| A、装置甲:除去乙烯中混有的少量SO2 |
| B、装置乙:用浓硫酸配制1mol/L的硫酸 |
| C、装置丙:检验HCl气体在水中的溶解性 |
| D、装置丁:用铜和浓硝酸反应制取NO2 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.乙烯可被酸性高锰酸钾溶液氧化生成二氧化碳气体;
B.容量瓶只能用于配制一定浓度的溶液,不能用于稀释浓硫酸;
C.根据气球的变化可判断HCl的溶解性;
D.二氧化氮和水反应,不能用排水法收集.
B.容量瓶只能用于配制一定浓度的溶液,不能用于稀释浓硫酸;
C.根据气球的变化可判断HCl的溶解性;
D.二氧化氮和水反应,不能用排水法收集.
解答:
解:A.乙烯可被酸性高锰酸钾溶液氧化生成二氧化碳气体,应用氢氧化钠溶液除杂,故A错误;
B.容量瓶只能用于配制一定浓度的溶液,不能用于稀释浓硫酸,应在烧杯中稀释并冷却后再转移到容量瓶中,故B错误;
C.如氯化氢极易溶于水,挤压胶头滴管内的水,烧瓶内压强减小,气球体积增大,故C正确;
D.二氧化氮和水反应,不能用排水法收集,只能用排水法收集,故D错误.
故选C.
B.容量瓶只能用于配制一定浓度的溶液,不能用于稀释浓硫酸,应在烧杯中稀释并冷却后再转移到容量瓶中,故B错误;
C.如氯化氢极易溶于水,挤压胶头滴管内的水,烧瓶内压强减小,气球体积增大,故C正确;
D.二氧化氮和水反应,不能用排水法收集,只能用排水法收集,故D错误.
故选C.
点评:本题考查较为综合,涉及物质的检验和性质的比较,综合考查学生的分析能力、实验能力和评价能力,为高考常见题型,注意把握物质的性质的异同以及实验的严密性和可行性的评价,难度不大.

练习册系列答案
相关题目
几种短周期元素的原子半径及主要化合价见下表:
则下列叙述中不正确的是( )
| 元素符号 | A | B | C | D | E | F |
| 原子半径(nm) | 0.160 | 0.080 | 0.102 | 0.143 | 0.074 | 0.125 |
| 主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 | +4 |
| A、B元素的金属性比A元素的强 |
| B、E与F形成的化合物是原子晶体 |
| C、C与E形成的化合物是分子晶体 |
| D、E的氢化物比C的氢化物沸点高 |
设NA为阿伏加德罗常数的值,下列叙述错误的是( )
| A、18g H2O中含有的质子数为10NA |
| B、1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
| C、46g NO2和N2O4混合气体中含有原子总数为3NA |
| D、常温常压下,22.4L N2和O2的混合气体中含有的分子数目为NA |
用NA表示阿伏德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4L SO3中含有的分子数为NA |
| B、2L 0.5mol/L的CH3COOH溶液中,含有CH3COO-离子个数为NA |
| C、常温常压下,3.4g NH3含有原子的数目为0.8NA个 |
| D、78g Na2O2与足量水反应转移的电子数目为2NA |
下列有关说法正确的是( )
| A、用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物 |
| B、镀锌铁板是利用了牺牲阳极的阴极保护法来达到防止腐蚀的目的 |
| C、取一定量水垢加盐酸,生成能使澄清石灰水变浑浊的气体,说明水垢的主要成分为CaCO3、MgCO3 |
| D、已知Cu2O+2H+═Cu2++Cu+H2O,氢气还原氧化铜后所得红色固体能完全溶于稀硝酸,说明还原产物是铜 |
下列简单实验方案,不能实现实验目的是( )
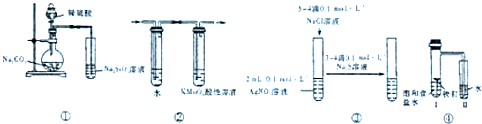

| A、①验证硫酸、碳酸、硅酸酸性强弱 |
| B、②检验溴乙烷发生消去反应生成的乙烯 |
| C、③验证AgCl沉淀能转化为溶解度更小的Ag2S沉淀 |
| D、④证明铁钉发生吸氧腐蚀 |
 材料的不断发展可以促进社会进步.
材料的不断发展可以促进社会进步.