题目内容
2.在由铜片、锌片和200mL稀硫酸组成的原电池中,若锌片只发生电化学腐蚀,在铜片上放出3.36L(标准状况下)的氢气时,硫酸恰好用完,则:(1)生成这些气体消耗的锌的质量是多少?
(2)通过导线的电子的物质的量是多少?
分析 该原电池中,锌电极上电极反应式为Zn-2e-=Zn2+,铜电极上电极反应式为2H++2e-=H2↑,则电池反应式为Zn+2H+=H2↑+Zn2+,
(1)根据氢气和锌之间的关系式计算锌的质量;
(2)根据氢气和转移电子之间的关系式计算转移电子的物质的量.
解答 解:(1)设锌片的质量减少了x,
Zn+H2SO4=ZnSO4+H2↑
65g 22.4L
x 3.36L
所以 x=9.75g,
答:锌片的质量减少了9.75g;
(2)设转移电子z,则
2H++2e-=H2↑
2mol 22.4L
y 3.36L
y=$\frac{2×3.36}{22.4}$mol=0.3mol
答:通过导线的电子的物质的量是0.3mol.
点评 本题以原电池为载体考查了氧化还原反应的有关计算,侧重于学生的分析能力和计算能力的考查,注意把握原电池的工作原理,明确各物理量间的关系是解本题的关键.

练习册系列答案
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案
相关题目
10.下列说法正确的是( )
| A. | 决定反应速率的因素只有催化剂 | |
| B. | 食物放在冰箱中会减慢食物变质的速率 | |
| C. | 锌与稀硫酸反应时,加入少量水能加快产生氢气的速率 | |
| D. | 在一定条件下2mol SO2与 1mol O2混合一定能生成2mol SO3 |
17.已知氯化铵的电子式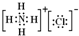 .下列有关氯化铵的叙述中,正确的是( )
.下列有关氯化铵的叙述中,正确的是( )
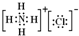 .下列有关氯化铵的叙述中,正确的是( )
.下列有关氯化铵的叙述中,正确的是( )| A. | 属于离子化合物 | B. | 属于共价化合物 | C. | 只含有离子键 | D. | 只含有共价键 |
7.羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制得. 下列有关说法正确的是( )


| A. | 苯酚和羟基扁桃酸互为同系物 | |
| B. | 常温下,1mol羟基扁桃酸只能与1mol Br2反应 | |
| C. | 乙醛酸的核磁共振氢谱中只有1个吸收峰 | |
| D. | 羟基扁桃酸可以发生取代、氧化、加成等反应 |
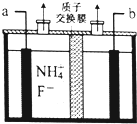 (1)某催化剂可将汽车尾气中的CO、NO转化为无毒气体.已知:
(1)某催化剂可将汽车尾气中的CO、NO转化为无毒气体.已知: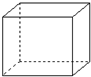 有机物的结构可用“键线式”简化表示.例如CH3-CH=CH-CH3可简写为
有机物的结构可用“键线式”简化表示.例如CH3-CH=CH-CH3可简写为  .“立方烷”是一种新合成的烃,其分子为正方体结构,其碳架结构如图:
.“立方烷”是一种新合成的烃,其分子为正方体结构,其碳架结构如图: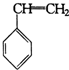 B.
B. 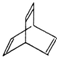 C.
C.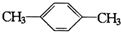 D.
D.
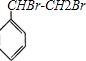 .
.