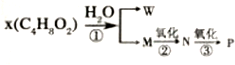题目内容
12. (1)某催化剂可将汽车尾气中的CO、NO转化为无毒气体.已知:
(1)某催化剂可将汽车尾气中的CO、NO转化为无毒气体.已知:2CO(g)+O2(g═2CO2(g)△H1=akJ.mol-1
N2(G)+O2(G)═2NO(g)△H2=bkJ.mol-1
①反应2NO(g)+2CO(g)?N2(g)+2CO2(g)的△H=a-bkJ.mol-1
②可以利用反应:NO2+G$\stackrel{催化剂}{→}$N2+H2O+nX(n可以为零)将NO2变成无害N2,若要求X必须为无污染的物质,则G可以是ad(填写字母).
a.NH3 b.CO2 c.SO2 d.CH3CH2OH
当反应中转移1.2mol电子时,消耗NO26.72L(标准状况).•
③用NaOH溶液吸收工业尾气中的SO2最终制得石膏(CaSO4•2H2O).为节约资源减少排放实现物质的循环利用,生产过程中还需要加入的固体物质是CaO或Ca(OH)2(填化学式).
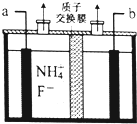
(2)工业上通过电解含NH4F的无水熔融物生产NF3气体,其电解原理如右图所示.则a极为阳极,该极的电极反应式NH4++3F--6e-=NF3+4H+
(3)用电镀法在铁板表面镀锌或锡可防腐,这种防止金属腐蚀的方法从原理上属于覆盖保护层法.
分析 (1)①2CO(g)+O2(g═2CO2(g)△H1=akJ.mol-1 (i),N2(G)+O2(G)═2NO(g)△H2=bkJ.mol-1 (ii),(i)-(ii)得出目标方程式;
②根据氧化还原反应中氧化剂和还原剂的特点结合常见的氧化剂和还原剂来回答;
③石膏中含有元素Ca,结合反应原理判断固体物质即可;
(2)由图可知,氢离子在b极得到电子生成氢气,故b为阴极,那么a为阳极,据此解答即可;
(3)依据常见金属保护方法回答即可.
解答 解:(1)①2CO(g)+O2(g═2CO2(g)△H1=akJ.mol-1 (i),N2(G)+O2(G)═2NO(g)△H2=bkJ.mol-1 (ii),(i)-(ii)得出目标方程式为:2NO(g)+2CO(g)?N2(g)+2CO2(g),故△H=(a-b)kJ.mol-1,故答案为:a-b;
②将NO2变成无害的N2中,氮元素的化合价降低了,二氧化氮做氧化剂,需要加入还原剂,X必须为无污染的物质,在下列四种物质:a.NH3 b.CO2 c.SO2 d.CH3CH2OH中,能被二氧化氮氧化具有还原性的物质有乙醇和NH3,NO2由+4价降低为0价,降低4价,即转移4mol电子,当反应中转移1.2mol电子时,消耗NO2 为0.3mol,体积为6.72L,故答案为:还原剂;ad;6.72;
③二氧化硫为酸性气体,除利用氢氧化钠浓溶液吸收外,还可以利用CaO或氢氧化钙吸收制取石膏,故还需要的固体物质是CaO或Ca(OH)2,故答案为:CaO或Ca(OH)2;(2)由图可知,氢离子在b极得到电子生成氢气,故b为阴极,那么a为阳极,阳极上铵根失去电子生成NF3,电极反应方程式为:NH4++3F--6e-=NF3+4H+,
故答案为:阳;NH4++3F--6e-=NF3+4H+;
(3)用电镀法在铁板表面镀锌或锡可防腐,这种防止金属腐蚀的方法从原理上属于覆盖保护层法,故答案为:覆盖并保护层.
点评 本题主要考查的是盖斯定律的应用、氧化还原反应方程式书写、电解池反应原理等,综合性较强,难度较大,注意整理归纳.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 碳酸钠(固体) | B. | 水 | C. | 硫酸钾溶液 | D. | 浓硝酸 |
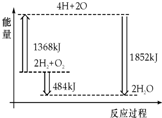
| A. | H2(g)和O2(g)反应生成H2O(g ),这是吸热反应 | |
| B. | 2 mol H2和1 mol O2转化为4 mol H、2 mol O原子的过程中放出热量 | |
| C. | 2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O( g),共放出484 kJ能量 | |
| D. | 4 mol H、2 mol O生成2 mol H2O(g),共放出484 kJ能量 |
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
 ;
;(2)在短周期中,元素的最高价氧化物对应的水化物中酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3;
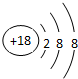
(3)在②⑦⑩元素中,原子半径最大的是Br,原子半径最小的是F;
(4)在③与⑨的单质中,化学性质较活泼的是K,写出其与水反应的化学方程式:2K+2H2O=2KOH+H2↑.
| A. | 常温下,1L 1mol•L-1的NH4NO3溶液中氮原子数为0.2NA | |
| B. | 1mol羟基中电子数为10NA | |
| C. | 在反应中,每生成3mol I2转移的电子数为6NA | |
| D. | 常温常压下,22.4L乙烯中C-H键数为4NA |
| A. | 乙酸溶液中存在乙酸分子,能证明乙酸是一种弱酸 | |
| B. | 丙醛和乙醛都有醛基,都能和银氨溶液、新制氢氧化铜反应 | |
| C. | 除去工业乙醇中少量水常加入生石灰,并蒸馏 | |
| D. | 油脂、淀粉、蛋白质、纤维素属于天然高分子化合物 |
| A. | 玻璃钢 | B. | 陶瓷 | C. | 二氧化硅 | D. | 聚乙烯 |
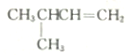 3-甲基-1-丁烯.
3-甲基-1-丁烯.