题目内容
13. 有机物的结构可用“键线式”简化表示.例如CH3-CH=CH-CH3可简写为
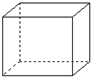
有机物的结构可用“键线式”简化表示.例如CH3-CH=CH-CH3可简写为  .“立方烷”是一种新合成的烃,其分子为正方体结构,其碳架结构如图:
.“立方烷”是一种新合成的烃,其分子为正方体结构,其碳架结构如图:(1)立方烷的分子式是C8H8
(2)该立方烷的二氯代物具有同分异构体的数目是3.
(3)有机物X是“立方烷”的同分异构体,且属于芳香烃,则X的结构简式为A(填符合条件的字母代号).
A.
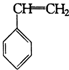 B.
B. 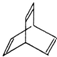 C.
C.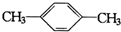 D.
D.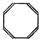
(4)X与乙烯一样也和溴水发生加成反应,写出X和溴水发生反应的化学方程式:
 +Br2→
+Br2→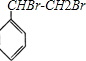 .
.
分析 (1)烃的键线式中交点、端点为碳原子,用H原子饱和C的四价结构,结合有机物键线式书写其分子式;
(2)烃的二氯代物的同分异构体可以采用固定一个氯原子的方法来寻找;
(3)芳香烃含有苯环,不饱度为5;
(4)双键变单键,并两端原子上各加上一个溴原子.
解答 解:(1)烃的键线式中交点、端点为碳原子,用H原子饱和C的四价结构,由有机物键线式可知,该有机物分子中由8个C原子、8个H原子,故其分子式为C8H8,
故答案为:C8H8;
(2)二氯代物的同分异构体分别是:一条棱、面对角线、体对角线上的两个氢原子被氯原子代替,所以二氯代物的同分异构体有三种,故答案为:3;
(3)芳香烃含有苯环,不饱度为5,符合条件的只有 ,故选A;
,故选A;
(4)溴水发生反应的化学方程式为: +Br2→
+Br2→ ,故答案为:
,故答案为: +Br2→
+Br2→ .
.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,题目难度不大,本题注意把握有机物的官能团的性质,注意把握同分异构体的判断,答题时注意审题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.如图为反应2H2(g)+O2(g)═2H2O(g)的能量变化示意图.下列说法正确的是( )
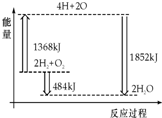

| A. | H2(g)和O2(g)反应生成H2O(g ),这是吸热反应 | |
| B. | 2 mol H2和1 mol O2转化为4 mol H、2 mol O原子的过程中放出热量 | |
| C. | 2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O( g),共放出484 kJ能量 | |
| D. | 4 mol H、2 mol O生成2 mol H2O(g),共放出484 kJ能量 |
4.下列说法不正确的是( )
| A. | 乙酸溶液中存在乙酸分子,能证明乙酸是一种弱酸 | |
| B. | 丙醛和乙醛都有醛基,都能和银氨溶液、新制氢氧化铜反应 | |
| C. | 除去工业乙醇中少量水常加入生石灰,并蒸馏 | |
| D. | 油脂、淀粉、蛋白质、纤维素属于天然高分子化合物 |
1.光导纤维常被用作制造石英表中的电压材料和高性能的现代通讯材料.下列物质中用于制造光导纤维的是( )
| A. | 玻璃钢 | B. | 陶瓷 | C. | 二氧化硅 | D. | 聚乙烯 |
8.下表是元素周期表的一部分,请回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为 .
.
(2)表中能形成两性氢氧化物的元素是Al (用元素符号表示),写出该元素的单质与⑨的最高价氧化物对应水化物反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(3)④元素与⑦元素形成化合物的化学式MgCl2.
(4)①、②、⑥、⑦四种元素的最高价氧化物对应水化物中酸性最弱的是H2CO3 (填化学式).
(5)③元素与⑩元素两者核电荷数之差是26.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
.(2)表中能形成两性氢氧化物的元素是Al (用元素符号表示),写出该元素的单质与⑨的最高价氧化物对应水化物反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(3)④元素与⑦元素形成化合物的化学式MgCl2.
(4)①、②、⑥、⑦四种元素的最高价氧化物对应水化物中酸性最弱的是H2CO3 (填化学式).
(5)③元素与⑩元素两者核电荷数之差是26.
5.某化学兴趣小组同学以TiO2和CCl4为原料在实验室制取液态TiCl4,装置如图所示.

有关信息如下:
①反应原理:TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$ TiCl4(g)+CO2(g)
②反应条件:无水无氧且加热
③有关物质性质如下表:
请回答下列问题:
(1)仪器A的名称是球形干燥管,其中装的试剂不可能是(填序号)B.
A.碱石灰 B.无水硫酸铜 C.氧化钙 D.烧碱
(2)整个实验过程中通N2的目的是排除装置中的空气,保证反应在无水无氧环境下进行.
(3)装置E中的试剂是浓硫酸;兴趣小组的甲同学认为实验中E装置不能换成A装置,理由是A装置不能吸收空气中的氧气,不能保证反应在无氧环境下进.
(4)实验开始前的操作包括:组装仪器、检查装置的气密性、加装药品、通N2一段时间后点燃酒精灯.
(5)欲分离D中的液态混合物,所采用操作的名称是蒸馏.
(6)TiCl4还可由TiO2和焦炭、氯气在加热下反应制得,同时有CO产生,反应的化学方程式为TiO2+2Cl2+2C $\frac{\underline{\;\;△\;\;}}{\;}$TiCl4+2CO;反应所需氯气可通过电解饱和食盐水制得,现电解1L饱和食盐水,当转移的电子数为0.1NA时,该溶液的pH值为13.

有关信息如下:
①反应原理:TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$ TiCl4(g)+CO2(g)
②反应条件:无水无氧且加热
③有关物质性质如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
(1)仪器A的名称是球形干燥管,其中装的试剂不可能是(填序号)B.
A.碱石灰 B.无水硫酸铜 C.氧化钙 D.烧碱
(2)整个实验过程中通N2的目的是排除装置中的空气,保证反应在无水无氧环境下进行.
(3)装置E中的试剂是浓硫酸;兴趣小组的甲同学认为实验中E装置不能换成A装置,理由是A装置不能吸收空气中的氧气,不能保证反应在无氧环境下进.
(4)实验开始前的操作包括:组装仪器、检查装置的气密性、加装药品、通N2一段时间后点燃酒精灯.
(5)欲分离D中的液态混合物,所采用操作的名称是蒸馏.
(6)TiCl4还可由TiO2和焦炭、氯气在加热下反应制得,同时有CO产生,反应的化学方程式为TiO2+2Cl2+2C $\frac{\underline{\;\;△\;\;}}{\;}$TiCl4+2CO;反应所需氯气可通过电解饱和食盐水制得,现电解1L饱和食盐水,当转移的电子数为0.1NA时,该溶液的pH值为13.

 ;
; ,该化合物所含化学键为共价键;
,该化合物所含化学键为共价键;