题目内容
3.乙烯是重要化工原料,其产量是一个国家石油化工发展水平的标志.请回答:(1)在一定条件下,乙烷和乙烯都能制备氯乙烷(C2H5Cl).
①用乙烷制备氯乙烷的化学方程式是CH3CH3+Cl2$\stackrel{光照}{→}$CH3CH2Cl+HCl,该反应的类型是取代反应.
②用乙烯制备氯乙烷的化学方程式是CH2=CH2+HCl→CH3CH2Cl,该反应的类型是加成反应.
比较上述两种方法,第②种方法更好.其原因是第①种方法生成的物质将是一系列混合物
第②种方法生成纯净的氯乙烷.
(2)此外,乙烯大量用来生产环氧乙烷,生产工艺主要有两种:
[工艺一]CH2═CH2+Cl2+Ca(OH)2→
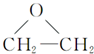 +CaCl2+H2O
+CaCl2+H2O[工艺二]2CH2═CH2+O2$\stackrel{Ag}{→}$
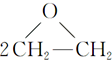
根据绿色化学的原则,理想的生产工艺是原子经济性好的反应,工艺一的原子利用率<100%(填“<”“=”或“>”,下同);工艺二的原子利用率=100%,因此,在实际生产中,采用工艺二更环保,更经济.
分析 (1)①根据烷烃与卤素单质在光照条件下发生取代反应得到卤代烃;②根据烯烃与卤化氢能发生加成反应得到卤代烃;根据产物是否纯净来解答;
(2)工艺一制取要经过多步反应制得,副产物多,原子利用率低;工艺二原子利用率为100%,原子利用率高.
解答 解:(1)①因烷烃与卤素单质在光照条件下发生取代反应得到卤代烃,所以用乙烷制备氯乙烷的化学方程式是CH3CH3+Cl2$\stackrel{光照}{→}$CH3CH2Cl+HCl,
故答案为:CH3CH3+Cl2$\stackrel{光照}{→}$CH3CH2Cl+HCl;取代反应;
②因烯烃与卤化氢能发生加成反应得到卤代烃,所以用乙烯制备氯乙烷的化学方程式是:CH2=CH2+HCl→CH3CH2Cl,
由乙烷与氯气在光照条件下发生反应得到的产物有:一氯乙烷,1,1-二氯乙烷,1,2-二氯乙烷,1,1,2-三氯乙烷,1,1,2,2-四氯乙烷,1,1,1,2-四氯乙烷,1,1,1,2,2-五氯乙烷,六氯乙烷和氯化氢,产物不唯一,而乙烯和卤化氢能发生加成反应得到氯乙烷,产物只有一种,
故答案为:CH2=CH2+HCl→CH3CH2Cl;加成反应;②;第①种方法生成的物质将是一系列混合物,第②种方法生成纯净的氯乙烷;
(2)工艺一除生成环氧乙烷外还有CaCl2和H2O的生成,副产物多,原子利用率低;工艺二乙烯和氧气反应全部生成了环氧乙烷,原子利用率为100%,原子利用率高;工艺二:乙烯和氧气反应全部生成了环氧乙烷,原子利用率为100%,符合绿色化学的原则,故选工艺二;
故答案为:<;=;二.
点评 本题考查了有机物的制备和方案的评价,题目难度不大,注意对有机物结构和性质的掌握.

练习册系列答案
相关题目
2.Fe3+、SO42-、Al3+和X四种离子以物质的量之比2:4:1:1大量共存于同一溶液中,X可能是( )
| A. | Br- | B. | OH- | C. | HCO3- | D. | NH4+ |
14.现代工业常以氯化钠、二氧化碳和氨气为原料制备纯碱,部分工艺流程如图:

有关说法错误的是( )

有关说法错误的是( )
| A. | 反应Ⅰ原理为CO2+NH3+NaCl+H2O→NaHCO3↓+NH4Cl | |
| B. | 向饱和NaCl溶液中先通入足量的CO2,再通入足量的NH3 | |
| C. | 反应Ⅰ生成的沉淀,经过过滤、洗涤、煅烧可得到纯碱 | |
| D. | 往母液中通入氨气,加入细小的食盐颗粒并降温,可使氯化铵析出 |
8.X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族,其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9.单质Y和W都可与浓的NaOH溶液反应.下列说法不正确的是( )
| A. | 原子半径:Y>Z>W | |
| B. | ZW2电子式为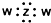 | |
| C. | 片状Y在空气中点燃时现象不剧烈 | |
| D. | 已知XW2熔点为-107℃、沸点为12.5℃,熔融时不导电,可说明固态XW2为共价化合物 |
12.下列说法正确的是( )
| A. | 任何化学反应,只要是放热反应,理论上都能设计成原电池 | |
| B. | 周期表中所有元素都是从自然界中发现的 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 原子结合成分子过程中一定释放出能量 |
13.某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理.
(1)请写出SO2与过量NaOH溶液反应的离子方程式:SO2+2OH-=H2O+SO32-.
(2)吸收尾气(Cl2)一段时间后,吸收液(强碱性)中肯定存在的阴离子有OH-和Cl-、SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响)
①提出合理假设.
假设1:只存在SO32-
假设2:既不存在SO32-,也不存在ClO-;
假设3:两种离子都存在(或者 只存在ClO-);.
②要证明假设1是否成立,设计实验方案,进行实验.请写出实验以及预期现象和结论.限选实验试剂:3mol•L-1H2SO4、1mol•L-1NaOH、0.01mol•L-1KMnO4、淀粉-KI溶液.
(1)请写出SO2与过量NaOH溶液反应的离子方程式:SO2+2OH-=H2O+SO32-.
(2)吸收尾气(Cl2)一段时间后,吸收液(强碱性)中肯定存在的阴离子有OH-和Cl-、SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响)
①提出合理假设.
假设1:只存在SO32-
假设2:既不存在SO32-,也不存在ClO-;
假设3:两种离子都存在(或者 只存在ClO-);.
②要证明假设1是否成立,设计实验方案,进行实验.请写出实验以及预期现象和结论.限选实验试剂:3mol•L-1H2SO4、1mol•L-1NaOH、0.01mol•L-1KMnO4、淀粉-KI溶液.
| 实验 | 预期现象和结论 |
| 取少许吸收液于试管中滴加1~2滴0.01mol•L-1KMnO4溶液 | 若溶液褪色则假设1成立,否则假设1不成立 |