题目内容
13.某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理.(1)请写出SO2与过量NaOH溶液反应的离子方程式:SO2+2OH-=H2O+SO32-.
(2)吸收尾气(Cl2)一段时间后,吸收液(强碱性)中肯定存在的阴离子有OH-和Cl-、SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响)
①提出合理假设.
假设1:只存在SO32-
假设2:既不存在SO32-,也不存在ClO-;
假设3:两种离子都存在(或者 只存在ClO-);.
②要证明假设1是否成立,设计实验方案,进行实验.请写出实验以及预期现象和结论.限选实验试剂:3mol•L-1H2SO4、1mol•L-1NaOH、0.01mol•L-1KMnO4、淀粉-KI溶液.
| 实验 | 预期现象和结论 |
| 取少许吸收液于试管中滴加1~2滴0.01mol•L-1KMnO4溶液 | 若溶液褪色则假设1成立,否则假设1不成立 |
分析 (1)氢氧化钠过量,二氧化硫和氢氧化钠反应生成亚硫酸钠和水;
(2)吸收尾气(Cl2)一段时间后,根据反应原理:Cl2+Na2SO3+2NaOH═2NaCl+Na2SO4+H2O,吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH- 和SO42-.①可假设1、溶液中可能存在只存在SO32,2、既不存在SO32-也不存在ClO-,3、SO32-、ClO-都存在或者只存在ClO-; ②3mol•L-1H2SO4硫酸电离生成氢离子,溶液显酸性,次氯酸根离子具有漂白性,亚硫酸根离子具有强的还原性,能被酸性的高锰酸钾氧化而使高锰酸钾褪色,选择具有强氧化性高锰酸钾溶液,证明SO32-的存在.
解答 解:(1)SO2与过量NaOH溶液反应,因NaOH过量,故生成的是正盐,化学方程式为:SO2+2NaOH=Na2SO3+H2O,离子方程式为:SO2+2OH-=H2O+SO32-,
故答案为:SO2+2OH-=H2O+SO32-;
(2)吸收尾气(Cl2)一段时间后,根据反应原理:Cl2+Na2SO3+2NaOH═2NaCl+Na2SO4+H2O,氯化钠、硫酸钠都为强电解质完全电离,所以吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH- 和SO42-,
故答案为:Cl-、SO42-;
①可假设1、溶液中可能存在只存在SO32,2、既不存在SO32-也不存在ClO-,3、SO32-、ClO-都存在或者只存在ClO-;
故答案为:两种离子都存在(或者只存在ClO-);
②因为吸收液呈碱性,先取少量吸收液于试管中,滴加3moL-L-1 H2SO4至溶液呈酸性,若存在SO32-,生成了H2SO3,H2SO3具有还原性,选择具有强氧化性高锰酸钾溶液,
在试管中滴加0.01mol•L-1KMnO4溶液1~2滴,若紫红色褪去,证明有SO32-,否则无,
故答案为:
| 实验 | 预期现象和结论 |
| 取少许吸收液于试管中滴加1~2滴0.01mol•L-1KMnO4溶液 | 若溶液褪色则假设1成立,否则假设1不成立 |
点评 本题属于实验探究题,要根据实验原理提出假设,再利用物质的性质加以验证,明确物质的性质是解题关键,(2)题为难点,注意依据反应产物的性质设计实验,利用亚硫酸的还原性验证是否含有亚硫酸根离子,题目难度中等.

 科学实验活动册系列答案
科学实验活动册系列答案| A. | IA族金属元素是同周期中金属性最强的元素 | |
| B. | 非金属元素组成的化合物中只含共价键 | |
| C. | 同种元素的原子均有相同的质子数和中子数 | |
| D. | VIIA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强 |
| A. | 20mL 3mol/L 的X溶液 | B. | 20mL 2mol/L 的X溶液 | ||
| C. | 10mL 4mol/L的X溶液 | D. | 10mL 2mol/L的X溶液 |
| A. | 当12NA个电子转移时,该反应放出1411 kJ的能量 | |
| B. | 当2NA个水分子生成且为液体时,放出1411 kJ的能量 | |
| C. | 当8NA个碳氧共用电子对生成时,放出1411 kJ的能量 | |
| D. | 当8NA个碳氧双键生成时,放出1411 kJ的能量 |
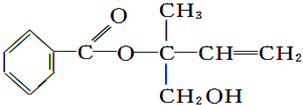
| A. | X的分子式为C12H16O3 | |
| B. | 可用酸性高锰酸钾溶液区分苯和X | |
| C. | X在一定条件下能发生水解、酯化、加成等反应 | |
| D. | 在Ni作催化剂的条件下,1 mol X最多只能与1 mol H2加成 |
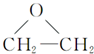 +CaCl2+H2O
+CaCl2+H2O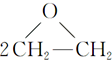
 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$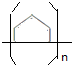 .
.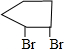 +2NaOH$→_{△}^{乙醇}$
+2NaOH$→_{△}^{乙醇}$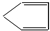 +2NaBr+2H2O.
+2NaBr+2H2O.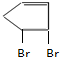 、
、 .
.