题目内容
18.下列实验设计能够成功的是( )| A. | 检验亚硫酸钠试样是否变质:试样$\stackrel{溶解}{→}$滴加$\stackrel{硝酸钡溶液}{→}$白色沉淀滴加$\stackrel{稀盐酸}{→}$沉淀不溶解-→说明试样已变质 | |
| B. | 除去粗盐中硫酸钙杂质:粗盐$\stackrel{溶解}{→}$足量$\stackrel{碳酸钠溶液}{→}$足量$\stackrel{氯化钡}{→}$溶液$\stackrel{过滤}{→}$滤液中$\stackrel{滴加}{→}$盐酸$\stackrel{结晶}{→}$精盐 | |
| C. | 检验某溶液中是否含有Fe2+试样$\stackrel{KSCN溶液}{→}$溶液颜色无变化$\stackrel{滴加氨水}{→}$溶液变红色-→溶液中含有Fe2+ | |
| D. | 证明酸性条件H2O2的氧化性比I2强:NaI溶液30%$\stackrel{H_{2}O_{2}}{→}$稀硝酸$\stackrel{淀粉}{→}$溶液变蓝色-→氧化性:H2O2>I2 |
分析 A.应先加盐酸,排除亚硫酸根离子的干扰;
B.应先加氯化钡,再加碳酸钠;
C.亚铁离子遇KSCN溶液不变色,亚铁离子被氧化生成铁离子遇KSCN溶液变色;
D.硝酸具有强氧化性,可氧化碘离子.
解答 解:A.若变质生成硫酸钠,应先加盐酸,排除亚硫酸根离子的干扰,再加氯化钡检验硫酸钠的存在,故A错误;
B.应先加氯化钡,再加碳酸钠,然后过滤后再加盐酸可实现除杂,选项B中钡离子不能除去,故B错误;
C.亚铁离子遇KSCN溶液不变色,滴加氯水后亚铁离子被氧化生成铁离子遇KSCN溶液变色,可证明溶液中含有Fe2+,故C正确;
D.硝酸具有强氧化性,可氧化碘离子,不能说明H2O2的氧化性比I2强,应选盐酸,故D错误;
故选C.
点评 本题考查物质的检验和鉴别实验方案的设计,为高频考点,把握常见离子的检验方法为解答的关键,注意离子检验中排除干扰及试剂的加入顺序,选项D为易错点,题目难度不大.

练习册系列答案
相关题目
6.完全燃烧3.2g某有机物,生成8.8g 二氧化碳和7.2g 水,关于该有机物的说法正确的是( )
| A. | 只含有碳、氢两种元素,不含氧元素 | |
| B. | 肯定含碳、氢两种元素,可能含氧元素 | |
| C. | 含碳、氢两种元素,且两者的质量比为11:9 | |
| D. | 含碳、氢、氧三种元素,且三者的质量比为8:1:16 |
13.汽车尾气主要的危害是形成光化学烟雾,危害人类健康.HNCO可用于消除汽车尾气中的NO和NO2,其反应原理为:HNCO+NOx→N2+CO2+H2O,下列说法正确的是( )
| A. | CO2分子中既含有极性键又含有非极性键 | |
| B. | 4.3g HNCO中含有0.1NA个原子 | |
| C. | 反应中NOx是还原剂 | |
| D. | 若NOx中x=2,1mol NO2在反应中转移4NA个电子 |
3.食品中常用到一些添加剂,其中NaHCO3属于( )
| A. | 氧化物 | B. | 盐 | C. | 碱 | D. | 酸 |
7.下列关于化学的认识说法不正确的是( )
| A. | 化学是在原子、分子水平上研究物质的组成和性质等 | |
| B. | 化学在能源和资源的合理利用等方面有着重要作用 | |
| C. | 化学是一门对人类生产和生活有着重要作用的实用学科 | |
| D. | 随着现代技术的发展,理论研究可以逐渐代替实验手段 |
13.下列关于强弱电解质的说法中,正确的是( )
| A. | Al2O3在熔化状态下全部电离,因而是弱电解质 | |
| B. | 具有极性键的共价化合物都是强电解质 | |
| C. | 具有非极性键的共价化合物都是弱电解质 | |
| D. | 所有弱酸、弱碱都是弱电解质 |
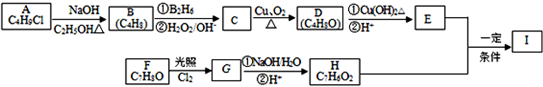
 ;
;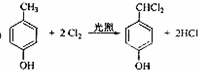 ;
; .
.