题目内容
9.化合物Ⅰ(C11H12O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基.Ⅰ可以用E 和H在一定条件下合成: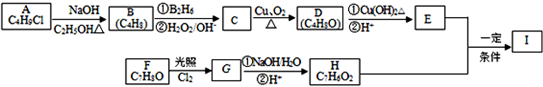
已知:①A的核磁共振氢谱表明其只有一种化学环境的氢;
②RCH=CH2$→_{②H_{2}O_{2}/OH-}^{①B_{2}H_{6}}$RCH2CH2OH
③化合物F苯环上的一氯代物只有两种;
④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基.
(1)A的化学名称为2-甲基-2-氯丙烷;
(2)D的结构简式为(CH3)2CHCHO;
(3)I的结构简式为
 ;
;(4)写出下列反应的类型:A→B:消去反应; C→D:氧化反应
(5)F生成G的化学方程式为:
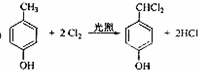 ;
;(6)I的同系物J比I相对分子质量小14,J能同时满足如下条件:①苯环上只有两个取代基,②能发生银镜反应,③能和饱和NaHCO3溶液反应放出CO2;符合上述条件的同分异构体共有18种(不考虑立体异构).若J的一个同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式
 .
.
分析 A中不含不饱和键,A的核磁共振氢谱表明其只有一种化学环境的氢,则A的结构简式为(CH3)3CCl,A和NaOH的醇溶液发生消去反应生成B,B结构简式为(CH3)2C=CH2,B发生加成反应生成C,C结构简式为(CH3)2CH2CH2OH,C在Cu作催化剂条件下发生氧化反应生成D,D结构简式为(CH3)2CH2CHO,D和新制氢氧化铜悬浊液发生氧化反应然后酸化得到E,E结构简式为(CH3)2CH2COOH;化合物F苯环上的一氯代物只有两种,则F结构简式为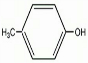 ,对甲基苯酚和氯气发生取代反应生成G,G发生取代反应生成H,结合题给信息、G和H分子式知,H中含有醛基,则F中甲基上氢原子被氯原子取代,G结构简式为
,对甲基苯酚和氯气发生取代反应生成G,G发生取代反应生成H,结合题给信息、G和H分子式知,H中含有醛基,则F中甲基上氢原子被氯原子取代,G结构简式为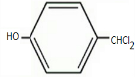 ,H结构简式为
,H结构简式为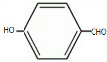 ,E和H发生酯化反应生成I,I结构简式为
,E和H发生酯化反应生成I,I结构简式为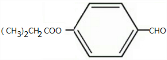 ,据此分析解答.
,据此分析解答.
解答 解:A中不含不饱和键,A的核磁共振氢谱表明其只有一种化学环境的氢,则A的结构简式为(CH3)3CCl,A和NaOH的醇溶液发生消去反应生成B,B结构简式为(CH3)2C=CH2,B发生加成反应生成C,C结构简式为(CH3)2CH2CH2OH,C在Cu作催化剂条件下发生氧化反应生成D,D结构简式为(CH3)2CH2CHO,D和新制氢氧化铜悬浊液发生氧化反应然后酸化得到E,E结构简式为(CH3)2CH2COOH;化合物F苯环上的一氯代物只有两种,则F结构简式为 ,对甲基苯酚和氯气发生取代反应生成G,G发生取代反应生成H,结合题给信息、GH分子式知,H中含有醛基,则F中甲基上氢原子被氯原子取代,G结构简式为
,对甲基苯酚和氯气发生取代反应生成G,G发生取代反应生成H,结合题给信息、GH分子式知,H中含有醛基,则F中甲基上氢原子被氯原子取代,G结构简式为 ,H结构简式为
,H结构简式为 ,E和H发生酯化反应生成I,I结构简式为
,E和H发生酯化反应生成I,I结构简式为 ,
,
(1)由上述分析可知,A为(CH3)3CCl,化学名称为:2-甲基-2-氯丙烷,
故答案为:2-甲基-2-氯丙烷;
(2)由上述分析可知,D的结构简式为(CH3)2CHCHO,
故答案为:(CH3)2CHCHO;
(3)I的结构简式为 ,
,
故答案为: ;
;
(4)根据上面的分析可知,A→B反应为消去反应,C→D反应为氧化反应,
故答案为:消去反应;氧化反应;
(5)F与氯气在光照条件下发生取代反应生成G为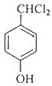 ,则F生成G的化学方程式
,则F生成G的化学方程式 ,
,
故答案为: ;
;
(6)I( )的同系物J比I相对分子质量小14,J比I少一个-CH2-原子团,J的同分异构体中能同时满足如下条件:①苯环上只有两个取代基,②既能发生银镜反应,又能与饱和NaHCO3溶液反应放出CO2,则J的同分异构体含有-CHO、-COOH,
)的同系物J比I相对分子质量小14,J比I少一个-CH2-原子团,J的同分异构体中能同时满足如下条件:①苯环上只有两个取代基,②既能发生银镜反应,又能与饱和NaHCO3溶液反应放出CO2,则J的同分异构体含有-CHO、-COOH,
侧链为-CHO、-CH2CH2COOH,有邻、间、对三种位置,
侧链为-CHO、-CH(CH3)COOH,有邻、间、对三种位置,
侧链为-CH2CHO、-CH2COOH,有邻、间、对三种位置,
侧链为-CH2CH2CHO、-COOH,有邻、间、对三种位置,
侧链为-CH(CH3)CHO、-COOH,有邻、间、对三种位置,
侧链为-CH3、-CH(CHO)COOH,有邻、间、对三种位置,
故符合条件的同分异构体有6×3=18种,
J的一个同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,而J的同分异构体发生银镜反应并酸化后的产物苯环侧链至少有2种H原子,故产物中苯环上只有1种H原子,产物有2个-COOH,应还含有2个-CH2-,2个侧链相同且处于对位,产物中侧链为-CH2COOH,故符合条件的同分异构体结构简式为: ,
,
故答案为:18; .
.
点评 本题考查有机物推断,侧重考查学生分析推断能力,以A、F结合题给信息为突破口采用正向分析的方法进行推断,结合反应条件判断有机物结构,难点是同分异构体种类判断,题目难度中等.

 阅读快车系列答案
阅读快车系列答案
| A. | 蒸发、蒸馏、过滤、萃取 | B. | 过滤、蒸馏、蒸发、萃取 | ||
| C. | 过滤、蒸发、分液、蒸馏 | D. | 萃取、蒸馏、蒸发、过滤 |
| A. | C4H10 | B. | C3H6O | C. | CH4O | D. | C2H4Cl2 |
| A. | CO2溶于水形成碳酸,SiO2难溶于水 | |
| B. | 氯化氢通入可溶性碳酸盐溶液中放出气体,通入可溶性硅酸盐溶液中生成沉淀 | |
| C. | 高温下SiO2与碳酸钙、碳酸钠等固体反应生成CO2 | |
| D. | CO2通入可溶性硅酸盐中析出硅酸沉淀 |
| A. | M+N═R+Q | B. | M+2N═2R+Q | C. | 2M+N═R+4Q | D. | 2M+N═R+2Q |
| A. | K+、Al3+、SO42-、NH3•H2O | |
| B. | 在pH=12的溶液中:Na+、K+、AlO2-、CO32- | |
| C. | 在pH=1的溶液中:K+、I-、Cl-、NO3- | |
| D. | 饱和氯水中:Cl-、NO3-、Na+、SO32 |
| A. | 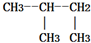 与 与 | B. | CH2=CH2与CH-CH3 | ||
| C. | 氢H和重氢D(${\;}_{1}^{1}$H与${\;}_{1}^{2}$H) | D. | 氧气与臭氧(O3) |
| A. | 检验亚硫酸钠试样是否变质:试样$\stackrel{溶解}{→}$滴加$\stackrel{硝酸钡溶液}{→}$白色沉淀滴加$\stackrel{稀盐酸}{→}$沉淀不溶解-→说明试样已变质 | |
| B. | 除去粗盐中硫酸钙杂质:粗盐$\stackrel{溶解}{→}$足量$\stackrel{碳酸钠溶液}{→}$足量$\stackrel{氯化钡}{→}$溶液$\stackrel{过滤}{→}$滤液中$\stackrel{滴加}{→}$盐酸$\stackrel{结晶}{→}$精盐 | |
| C. | 检验某溶液中是否含有Fe2+试样$\stackrel{KSCN溶液}{→}$溶液颜色无变化$\stackrel{滴加氨水}{→}$溶液变红色-→溶液中含有Fe2+ | |
| D. | 证明酸性条件H2O2的氧化性比I2强:NaI溶液30%$\stackrel{H_{2}O_{2}}{→}$稀硝酸$\stackrel{淀粉}{→}$溶液变蓝色-→氧化性:H2O2>I2 |

实验方法:在干燥的锥形瓶中放入称量好的水杨酸(6.2g 0.045mol)、乙酸酐(5mL 5.4g 0.053mol),滴入5滴浓硫酸,在70℃反应一段时间,按如下流程分离出乙酰水杨酸.
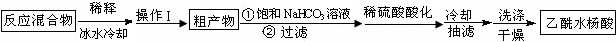
已知:①乙酰水杨酸溶于热水,在冷水中微溶;乙酸酐遇水生成乙酸.饱和NaHCO3溶液
②乙酰水杨酸钡、水杨酸钡均可溶于水.
(1)反应后用40mL冰水稀释反应混合物的操作是:待反应液稍冷后,在玻璃棒不断搅拌下将反应液沿烧杯壁慢慢倒入40ml冰水中.
(2)操作Ⅰ为过滤.
(3)判断粗产物与饱和碳酸氢钠反应完全的现象是:无气泡产生.
(4)某同学推测产品中可能还含有少量水杨酸和Na2SO4,设计了如下方案进行检验,实验证明不含杂质,请在答题卡上完成表中内容.
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将少量产品加入6mL水的试管A中,振荡,将上层液体倾析至B、C中. | 得到白色晶体和无色溶液 | |
| ② | 向试管B中,加入少量BaCl2溶液(或取试管B中溶液做焰色反应实验). 此空删去.此空删去 | 无白色沉淀生成 | 产品中不含SO42- |
| ③ | 向试管C中,加入少量FeCl3溶液(或浓溴水). 此空删去.此空删去 | 溶液不显紫色(或无白色沉淀出现). | 产品中不含水杨酸 |