题目内容
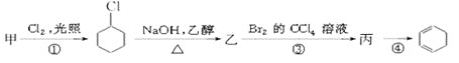
【题目】已知:链烃A(C5H8)有支链且只有一个官能团。有机化合物A~H的转换关系如下所示:
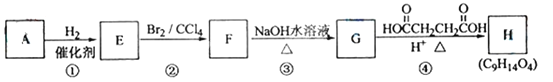
请回答下列问题:
(1)A的结构简式是_________________,名称是________________。
(2)链烃B是A的不同类别的同分异构体,B经催化氢化转化为正戊烷,写出B所有可能的结构简式_________________________________________________________。
(3)写出反应类型:反应②___________________,反应③____________________。
(4)写出反应④的化学方程式:_____________________________________________。
【答案】CH![]() C-CH(CH3)2 3-甲基-1-丁炔 CH3CH=CHCH=CH2 CH2=CHCH2CH=CH2 加成反应 水解反应(取代反应)
C-CH(CH3)2 3-甲基-1-丁炔 CH3CH=CHCH=CH2 CH2=CHCH2CH=CH2 加成反应 水解反应(取代反应) 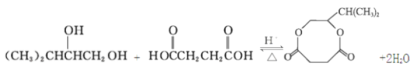
【解析】
链烃A(C5H8)有支链且只有一个官能团,根据结构式推断符合规律![]() ,则A是炔烃;反应①是加成反应;反E能与溴的四氯化碳溶液继续反应生成F,则E是烯烃:3-甲基-1-丁烯;F的结构简式是:
,则A是炔烃;反应①是加成反应;反E能与溴的四氯化碳溶液继续反应生成F,则E是烯烃:3-甲基-1-丁烯;F的结构简式是:![]() ,F到G是卤代烃的水解反应,生成醇。
,F到G是卤代烃的水解反应,生成醇。
(1) 链烃A(C5H8)有支链且只有一个官能团,且是炔烃,则A的结构简式是CH![]() C-CH(CH3)2,名称是3-甲基-1-丁炔;
C-CH(CH3)2,名称是3-甲基-1-丁炔;
(2) 链烃B是A的不同类别的同分异构体,B经是含两个碳碳双键的烯烃,又两个双键在同一个碳上不稳定,又B经催化氢化转化为正戊烷,则B可能的结构简式:CH3CH=CHCH=CH2 、CH2=CHCH2CH=CH2;
(3)由分析知,反应②是加成反应;反应③卤代烃的水解反应;
(4)反应④的化学方程式: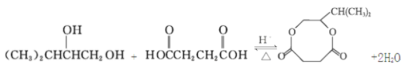 。
。

 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案【题目】下表为元素周期表的短周期部分。
a | |||||||
b | c | d | |||||
e | f | g | h |
请参照元素a-h在表中的位置,根据判断出的元素回答问题:
(1)h原子核外有 _____ 种不同伸展方向的电子云,最外层共有 _____ 种不同运动状态的电子。
(2)比较d、e元素常见离子的半径大小(用化学式表示)_______>__________;b、c 两元素非金属性较强的是(写元素符号)________,写出证明这一结论的一个化学方程式 ___________________ 。
(3)d、e元素形成的四原子化合物的电子式为___________;b、g元素形成的分子bg2为__________分子(填写“极性”或“非极性”)。
(4)上述元素可组成盐R:ca4f(gd 4)2和盐S:ca4agd4 ,相同条件下,0.1 mol/L 盐R中c(ca4+)________(填“等于”、“大于”或“小于”)0.1 mol/L 盐S中c(ca4+)。
(5)向盛有10mL1 mol/L盐S溶液的烧杯中滴加1 mol/L NaOH溶液至中性,则反应后各离子浓度由大到小的排列顺序是 __________________________________________ 。
(6)向盛有10mL 1 mol/L盐 R溶液的烧杯中滴加1 mol/L NaOH溶液32mL后,继续滴加至35mL写出此时段(32mL—35mL)间发生的离子方程式: _________________________ 。若在10mL 1 mol/L 盐R溶液的烧杯中加20mL1.2 mol/L Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为__________mol。
【题目】CO和H2可作为能源和化工原料,应用十分广泛。常利用煤气化过程中生成的CO和H2来制备甲醇。
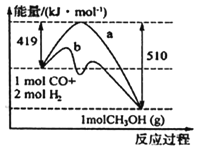
(1)请根据图示写出该反应的热化学方程式:_______________;图中使用催化剂曲线是_______(填“a”或“b”)。
(2)已知:C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
C(s)+H2O(g)=CO(g)+H2(g) ΔH2=+131.3 kJ/mol
则反应CO(g)+H2(g)+O2(g)=H2O(g)+CO2(g)的ΔH=______________kJ/mol。
(3)反应CO(g)+H2O(g)![]() H2(g)+CO2(g)的平衡常数随温度的变化如下表所示。
H2(g)+CO2(g)的平衡常数随温度的变化如下表所示。
温度/℃ | 400 | 500 | 830 | 1000 |
平衡常数K | 10 | 9 | 1 | 0.6 |
①从上表可以推断:此反应是__________(填“吸”或“放”)热反应。
②在830 ℃下,若开始时向恒容密闭容器中充入CO与H2O均为1 mol,则达到平衡后CO的转化率为___________________。
(4)汽车排气管上的催化转化器发生如下反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H<0,在一定温度下,将一定量的NO和CO充入2 L固定容积的容器中,回答以下问题:
N2(g)+2CO2(g) △H<0,在一定温度下,将一定量的NO和CO充入2 L固定容积的容器中,回答以下问题:
①能说明该反应达到平衡状态的是_____________(填字母标号)。
A. 2v正(NO)=v逆(N2) B. 混合气体的平均相对分子质量保持不变
C. 气体总压强不再变化 D. ΔH保持不变
E.混合气体的密度不再变化
②从反应开始到5 min,生成了0.08 mol N2,则5 min内v(CO)=__________mol/(L·min)。
③25 min时,物质浓度变化如图所示,则改变的条件可能是________(填字母标号)。
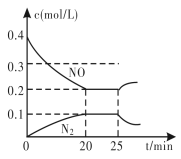
A. 缩小容器体积 B. 增加NO的浓度
C. 降低温度 D. 升高温度