题目内容
【题目】下列图示与对应的叙述相符的是

A.图I表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
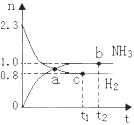
B.图Ⅱ表示常温下,0.1000mol/LNaOH溶液滴定20.00mL、0.0100mol/LHCl溶液所得到的滴定曲线
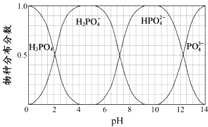
C.图Ⅲ表示一定质量的冰醋酸加水稀释过程中,醋酸溶液电离程度:c < a < b
D.图Ⅳ表示反应4CO(g)+2NO2(g) ![]() N2(g)+4CO2(g),在其他条件不变的情况下改变起始物CO的物质的量,平衡时N2的体积分数变化情况,由图可知NO2的转化率c > b > a
N2(g)+4CO2(g),在其他条件不变的情况下改变起始物CO的物质的量,平衡时N2的体积分数变化情况,由图可知NO2的转化率c > b > a
【答案】D
【解析】
A.吸热反应,反应物的总能量小于生成物的总能量,反应中加入催化剂会降低活化能,与图不符,A错误;
B.氢氧化钠滴定盐酸,盐酸属于强酸,0.0100mol/LHCl,HCl开始的pH为2,而图像中pH为1,所示盐酸的浓度为0.100mol/L,相互矛盾,B错误;
C.冰醋酸加水溶解,离子浓度增大,导电能力增强,达到平衡后继续加入水促进醋酸电离,但离子浓度减小导电能力减小,图象符合离子浓度变化,导电能能力b>a>c;根据越稀越电离,a、b、c三点醋酸的电离程度:a<b<c,C错误;
D.4CO(g)+2NO2(g)N2(g)+4CO2(g),在其它条件不变的情况下增大起始反应物CO的物质的量,二氧化氮转化率增大,NO2的转化率:c>b>a,D正确;
答案选D。

练习册系列答案
相关题目