题目内容
5.长周期中的某主族元素R,其原子核外最外电子层上只有1个电子,下列叙述中正确的是( )| A. | R的单质常温下跟水反应不如钠剧烈 | |
| B. | R的碳酸盐易溶于水 | |
| C. | R的原子半径比钾的原子半径小 | |
| D. | R的氢氧化物不能使氢氧化铝溶解 |
分析 长周期中的某主族元素R,其原子核外最外电子层上只有1个电子,则应为ⅠA族元素,反应中易失去电子,同主族元素从上到下,金属性逐渐增强,以此来解答.
解答 解:长周期中的某主族元素R,其原子核外最外电子层上只有1个电子,则应为ⅠA族元素,
A.钠为短周期元素,同主族元素从上到下,金属性逐渐增强,R的单质比钠活泼,故A错误;
B.碱金属元素对应的碳酸盐都易溶于水(碳酸锂除外),故B正确;
C.同主族元素从上到下原子半径逐渐增大,故C错误;
D.氢氧化铝可与强碱反应,R的氢氧化物能使氢氧化铝溶解,故D错误.
故选B.
点评 本题考查原子结构与元素的性质,为高频考点,题目难度不大,本题注意元素价层电子排布特点以及与在周期表位置的关系,熟练掌握元素周期表的结构.

练习册系列答案
相关题目
16.A、B、C三种短周期元素,已知A元素的原子最外层电子数等于其电子层数,B元素的原子最外层电子数是其电子层数的2倍,C元素的原子最外层电子数是其电子层数的3倍.由这三种元素组成的化合物的化学式不可能是( )
| A. | A3BC2 | B. | A4B2C | C. | A8B3C3 | D. | A4B2C2 |
13.对下列化学用语的理解正确的是( )
| A. | 结构示意图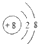 ,可以表示一种原子,也可以表示一种离子 ,可以表示一种原子,也可以表示一种离子 | |
| B. | 比例模型 可以表示二氧化碳分子,也可以表示二硫化碳分子分子 可以表示二氧化碳分子,也可以表示二硫化碳分子分子 | |
| C. | 电子式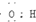 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 | |
| D. | 分子式C2H4O2:可以表示乙酸,也可以表示甲酸甲酯 |
10.下列说法不正确的是( )
| A. | 等体积等浓度的Na2S溶液和Na2SO3溶液中,离子数目以前者为多 | |
| B. | 已知室温时0.10mol/L NH4Cl溶液中c(H+)=7.5×10-6mol/L,室温时0.10mol/L KCN溶液中c (OH-)=1.3×10-3mol/L.那么此时0.10mol/L NH4CN溶液中pH>7 | |
| C. | 等pH、等体积的醋酸和硫酸,分别与足量的碳酸氢钠反应,在相同条件下,硫酸放出气体更多 | |
| D. | 醋酸加到氢氧化钠溶液中,若要使所得溶液呈中性,醋酸应稍过量 |
17.下列操作中,后者最终能被漂白的是( )
| A. | 将干燥的氯气与红色鲜花充分接触 | B. | 将H2 02加入到KMnO4溶液中 | ||
| C. | 将足量SO2通入紫色石蕊试液中 | D. | 将漂白液加入到Fe2(SO4)3溶液中 |
14.下列各组物质中,互为同位素的是( )
| A. | T2O与D2O | B. | 4019K与4020C | C. | O2和O3 | D. | 21H和31H |
15.中学化学中很多规律都有其适用范围,下列根据有关规律推出的结论合理的是( )
| A. | H2CO3的酸性比HClO强,推出CO2通入NaClO溶液中能生成HClO | |
| B. | SO2和湿润的C12都有漂白性,推出二者混合后漂白性更强 | |
| C. | Na2O、Na2O2组成元素相同,推出与水反应产物也完全相同 | |
| D. | CuCl2溶液与H2S可以生成CuS沉淀,推出FeCl2溶液也可与H2S生成FeS沉淀 |
