题目内容
15.中学化学中很多规律都有其适用范围,下列根据有关规律推出的结论合理的是( )| A. | H2CO3的酸性比HClO强,推出CO2通入NaClO溶液中能生成HClO | |
| B. | SO2和湿润的C12都有漂白性,推出二者混合后漂白性更强 | |
| C. | Na2O、Na2O2组成元素相同,推出与水反应产物也完全相同 | |
| D. | CuCl2溶液与H2S可以生成CuS沉淀,推出FeCl2溶液也可与H2S生成FeS沉淀 |
分析 A.化学反应遵循强酸制弱酸的规律;
B.二氧化硫和氯气在水溶液中会发生氧化还原反应;
C.氧化钠和水反应生成氢氧化钠,过氧化钠和水反应的产物有氢氧化钠和氧气;
D.化学反应遵循强酸制弱酸的规律.
解答 解:A.化学反应遵循强酸制弱酸的规律,将CO2通入NaClO溶液中能生成HClO,故A正确;
B.等物质的量的二氧化硫和氯气在水溶液中会发生氧化还原反应生成盐酸和硫酸,不再具有漂白性,故B错误;
C.氧化钠和水反应生成氢氧化钠,过氧化钠和水反应的产物有氢氧化钠和氧气,产物不一样,故C错误;
D.FeCl2与H2S生成FeS和氯化氢,不遵循强酸制弱酸的规律,故D错误.
故选A.
点评 本题考查化学反应的基本原理,涉及物质的性质方面的知识,难度适中,解题时要注意一般规律与特殊情况的关系,以及规律所适用的条件等.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
5.长周期中的某主族元素R,其原子核外最外电子层上只有1个电子,下列叙述中正确的是( )
| A. | R的单质常温下跟水反应不如钠剧烈 | |
| B. | R的碳酸盐易溶于水 | |
| C. | R的原子半径比钾的原子半径小 | |
| D. | R的氢氧化物不能使氢氧化铝溶解 |
6.下列说法正确的是( )
| A. | 已知:2H2(g)+O2(g)=2H2O(l)△H<0,反应物总能量小于生成物总能量 | |
| B. | 测定盐酸和氢氧化钠反应的中和热实验中,所用试剂可以是浓溶液 | |
| C. | HCl和NaOH反应的中和热△H=-57.3 kJ•mol-1,则1molH2SO4和1molBa(OH)2反应放出的热量为114.6kJ | |
| D. | 已知C(s)与CO(g)的燃烧热分别为393.5kJ•mol-1、283.0kJ•mol-1,则相同条件下C(s)与O2(g)反应生成1molCO(g)的反应热为△H=-110.5kJ/mol |
10.下列说法错误的是( )
| A. | FeO是碱性氧化物 | |
| B. | 用加热法分离泥沙中的碘单质是化学变化 | |
| C. | 丁达尔效应可用于区分胶体和溶液 | |
| D. | Fe2O3+3CO $\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3CO2 是复分解反应 |
7.上述反应中Z气体的化学计量数n的值是( )
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
4.下列关于物质的分类说法正确的是 ( )
| A. | 纯碱、烧碱都属于碱 | |
| B. | 漂白粉、小苏打都属于纯净物 | |
| C. | 氯化铵、次氯酸都属于电解质 | |
| D. | 合成纤维和光导纤维都是新型无机非金属材料 |
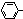 ):
):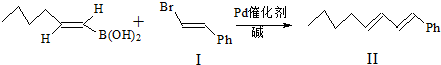
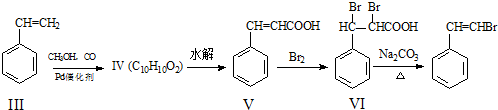
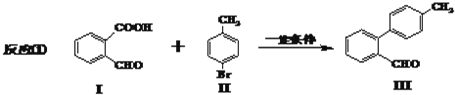
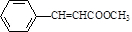 ,化合物V转化为化合物VI的反应类型为加成反应.
,化合物V转化为化合物VI的反应类型为加成反应. .
.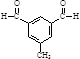 或
或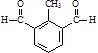 .
.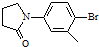 )与化合物(
)与化合物(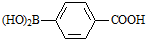 )能发生偶联反应生成一种抗抑郁药物,写出该抗抑郁药物的结构简式
)能发生偶联反应生成一种抗抑郁药物,写出该抗抑郁药物的结构简式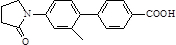 .
.
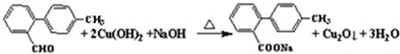 .
. (要求:①能与FeCl3溶液发生显色反应;②苯环上一氯取代产物有2种)
(要求:①能与FeCl3溶液发生显色反应;②苯环上一氯取代产物有2种)