��Ŀ����
1������ʯ[Ca3��PO4��2]��SiO2����̿Ϊԭ�Ͽ��������ס����ᡢ�״����轺�ȶ������ʣ�ͼ1�������̵���ƾ���ԭ�������ʸߣ��������ٵ��ص㣮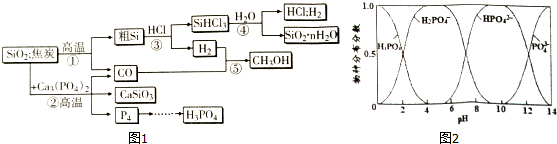
��1��̼���衢�ࡢǦΪͬ��Ԫ�أ���ԭ�ӵĺ�������Ų����ĸ��㣻������Ӧ�������û���Ӧ���Ǣ٢ۣ�
��2����ʯ[Ca3��PO4��2]��SiO2����̿�����������Ʊ����ף����������뻹ԭ�������ʵ�����Ϊ1��5��
����������ˮ���ú����ò�������ɵ���������ᣬд����Ӧ�Ļ�ѧ����ʽP4+16H2O+10Cl2=4H3PO4+20HCl��
��3����Ӧ����Ҫ�ڸ�����������ˮ�����½��У��������Ǹ���������������е������ᷢ����ը��
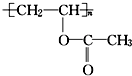
��4������Ҫ������NaH2PO4��Na2HPO4��Na3PO4��ͨ��H3PO4��NaOH��Һ��Ӧ��ã��������ֵķֲ�������ƽ��ʱij���ֵ�Ũ��ռ������Ũ��֮�͵ķ�������pH�Ĺ�ϵ��ͼ2��ʾ��pH=8����Һ�к��������ӵ�Ũ�ȴ�С��ϵΪc��HPO42-����c��H2PO4-�����ɵ�Ũ��NaH2PO4��Na2HPO4��ɵĻ����Һ�п�����ǿ�������ǿ��Ļ����ԣ�����Ϊ������Һ�������������������Һ����pH������������д���û����Һ�μ�����NaOH��Һʱ��Ҫ���Ӧ�����ӷ���ʽH2PO4-+OH-=HPO42-+H2O��
��5���״��Ϳ����ļ���ȼ�ϵ������ת���ʸߣ�1mol�״���ȫȼ�գ���Һ���պ�ų�����akJ����ȼ�ϵ�ص�����ת��Ч��Ϊ80%����ü״�ȼ�ϵ�ص������ܶ�Ϊ����λǧ������ȼ��ת��Ϊ����ʱ�ų�������25a��kJ/kg��
���� ��1�������������ڵ��Ӳ������û���Ӧ�ǵ����뻯���ﷴӦ������һ�ֵ�������һ�ֻ����
��2����ʯ[Ca3��PO4��2]��SiO2����̿�����������Ʊ����ף���Ӧ����ʽΪ��2Ca3��PO4��2+6SiO2+10C�T6CaSiO3+P4+10CO���ɸ��ݻ��ϼ۵ı仯�������жϣ�����������ˮ���ú����ò�������ɵ���������ᣬ��Ӧ����ʽΪ��P4+16H2O+10Cl2=4H3PO4+20HCl��
��3������������������е������ᷢ����ը��
��4����Һ����Ҫ��������Ũ�ȴ�С��ϵ����ͼ���ó�������������H+ʱ��HPO4-��H+��Ӧ������H+��HPO4-+H+=H2PO4-������������OH-ʱ��H2PO4-��OH-��Ӧ������OH-��H2PO4-+OH-=HPO42-+H2O��
��5��1mol�״���ȫȼ�գ���Һ���պ�ų�����akJ������2CH3OH+3O2+4KOH=2K2CO3+6H2O�ų�����Ϊ��0.8a����״�ȼ�ϵ�ص������ܶ�Ϊ$\frac{0.8a}{32��1{0}^{-3}}$=25a��
��� �⣺��1�������������ڵ��Ӳ�������λ�ڵ������ڣ����Ժ�������Ų����ĸ����Ӳ㣻���������뽹̿��Ӧ���ɹ���һ����̼�ʹֹ����Ȼ��ⷴӦ�����û���Ӧ���ʴ�Ϊ���ĸ����٢ۣ�
��2����ʯ[Ca3��PO4��2]��SiO2����̿�����������Ʊ����ף���Ӧ����ʽΪ��2Ca3��PO4��2+6SiO2+10C�T6CaSiO3+P4+10CO����Ӧ�����н�̿��̼Ԫ�صĻ��ϼ����ߣ�����ԭ����������е���Ԫ�ػ��ϼ۽��������������������뻹ԭ�������ʵ���֮��Ϊ��2��10���������������뻹ԭ�������ʵ�����Ϊ1��5������������ˮ���ú����ò�������ɵ���������ᣬ��Ӧ����ʽΪ��P4+16H2O+10Cl2=4H3PO4+20HCl��
�ʴ�Ϊ��1��5��P4+16H2O+10Cl2=4H3PO4+20HCl��
��3������������������е������ᷢ����ը������Ҫ�����������ʴ�Ϊ������������������е������ᷢ����ը��
��4����Һ����Ҫ��������Ũ���ȴ�С��ϵ����ͼ���ó� c��HPO42-����c��H2PO4-��������������H+ʱ��HPO4-��H+��Ӧ������H+��HPO4-+H+=H2PO4-������������OH-ʱ��H2PO4-��OH-��Ӧ������OH-��H2PO4-+OH-=HPO42-+H2O���ʴ�Ϊ��c��HPO42-����c��H2PO4-����H2PO4-+OH-=HPO42-+H2O��
��5��1mol�״���ȫȼ�գ���Һ���պ�ų�����akJ������2CH3OH+3O2+4KOH=2K2CO3+6H2O�ų�����Ϊ��0.8a����״�ȼ�ϵ�ص������ܶ�Ϊ$\frac{0.8a}{32��1{0}^{-3}}$=25akJ/kg���ʴ�Ϊ��25a��
���� ���⿼��Ԫ�ػ�����֮���ת�����Ԫ�������ɺͻ�ѧ��Ӧ�������Լ���ѧ��Ӧԭ���Ŀ��飬�ۺ���ǿ����һ�����Ѷȣ�

��������İٷֺ���һ�����ӣ���������IJ���һ�����ӣ� �۷�Ӧ���ת����һ������
�ܷ�Ӧ���Ũ��һ�����ͣ� ������Ӧ����һ�������淴Ӧ���ʣ���ʹ�ú��ʵĴ�����
| A�� | �٢� | B�� | �ڢ� | C�� | �ڢۢ� | D�� | �ڢۢܢݢ� |
 �й����Ƴɹ���ȫ��Ψһ������ű����Чҩ--�����أ���������������еġ��й���ҩ�����ṹ��ͼ��ʾ��Ŀǰ�ۼ�ÿ��225��Ԫ�����������15�֣�����������ʮ��֮һ������Ӧ�����й��������ص�˵����ȷ���ǣ�������
�й����Ƴɹ���ȫ��Ψһ������ű����Чҩ--�����أ���������������еġ��й���ҩ�����ṹ��ͼ��ʾ��Ŀǰ�ۼ�ÿ��225��Ԫ�����������15�֣�����������ʮ��֮һ������Ӧ�����й��������ص�˵����ȷ���ǣ�������| A�� | ��һ���� | B�� | ���ڸ߷��ӻ����� | ||
| C�� | ���ڷ����廯���� | D�� | ����ʽ��C15H22O5 |
| A�� | Fe2+��Mg2+��SO42-��NO3- | B�� | Na+��Ag+��Br-��PO43- | ||
| C�� | Ba2+��K+��SO32-��ClO- | D�� | Al3+��NH4+��CO32-��Cl- |
| A�� | �ӷ����⣬���⻯����ȶ������� | |
| B�� | ������Ϊͬ����Ԫ�أ��������ԭ�Ӱ뾶С��������ķǽ�����ǿ | |
| C�� | �������ڴ��Ƶ��ȣ�����������ˮ���������������������ǿ | |
| D�� | ��Ϊ��ԭ�ӱ���ԭ��ʧȥ������Ŀ�࣬���������ƵĻ�ԭ��ǿ |
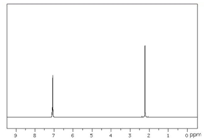
 �����й��ڸ��л�����������ȷ���ǣ�������
�����й��ڸ��л�����������ȷ���ǣ�������| A�� | 1 mol ���л����� NaOH ��Һ��ȫ��Ӧʱ������ NaOH 1 mol | |
| B�� | ���л���ˮ�����ò����ܷ���ȡ����Ӧ | |
| C�� | ���л����ͨ���Ӿ۷�Ӧ���� | |
| D�� | ���л�������к���˫�� |
| A�� | ˮ | B�� | ��ˮ�ƾ� | C�� | ���Ȼ�̼ | D�� | ����������Һ |
| A�� |  | B�� | 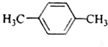 | C�� | 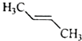 | D�� | 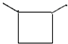 |
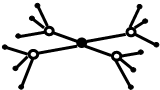 ���ڱ�ǰ�����ڵ�Ԫ��X��Y��Z��T��W��ԭ��������������X�ĺ����������������������ͬ��Y��̬ԭ�ӵ�p��������s��������1����Z��̬ԭ�ӵļ۵��Ӳ�����2��δ�ɶԵ��ӣ�T��Zͬ���壬W��̬ԭ�ӵ�M��ȫ������N��ֻ��һ�����ӣ��ش��������⣺
���ڱ�ǰ�����ڵ�Ԫ��X��Y��Z��T��W��ԭ��������������X�ĺ����������������������ͬ��Y��̬ԭ�ӵ�p��������s��������1����Z��̬ԭ�ӵļ۵��Ӳ�����2��δ�ɶԵ��ӣ�T��Zͬ���壬W��̬ԭ�ӵ�M��ȫ������N��ֻ��һ�����ӣ��ش��������⣺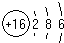 ��W��̬ԭ�ӵĵ����Ų�ʽΪ[Ar]3d104s1��
��W��̬ԭ�ӵĵ����Ų�ʽΪ[Ar]3d104s1��