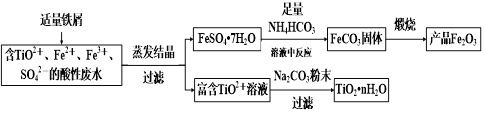
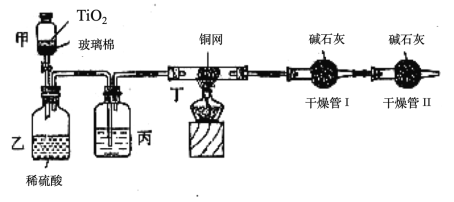
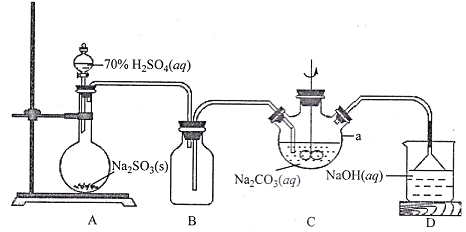
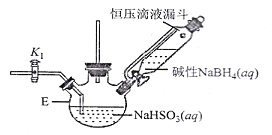
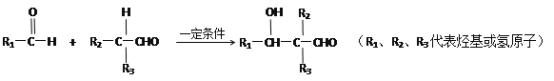
题目内容
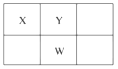
【题目】X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素。其中只有Z是金属元素,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图所示。下列说法正确的是( )
A.Z的最高价氧化物对应的水化物不可能显弱碱性
B.Y的简单阴离子比W的简单阴离子的还原性弱
C.元素Z、W、Q中原子半径最大的是Q
D.W的最高价氧化物对应的水化物浓溶液加热时不可能与铜反应
【答案】B
【解析】
因W单质时黄色固体,因此W为硫元素,结合位置关系可知Y为氧元素,X为氮元素,结合原子序数依次增大可知Q为氯元素,Z的原子序数介于8和16之间,且为金属元素,因此Z可能为钠、镁、铝中的一种。
A.若Z为金属铝,则其最高价氧化物的水化物氢氧化铝可以体现弱碱性,A项错误;
B.由于硫离子半径大于氧离子半径,因此氧离子还原性弱于硫离子,B项正确;
C.Z、W、Q为同周期元素,且Z的原子序数最小,因此Z的原子半径最大,C项错误;
D.W的最高价氧化物的水化物为硫酸,浓硫酸在加热条件下能够与金属铜反应,D项错误。
故答案选B。

 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案【题目】为测定Na2CO3和NaHCO3固体混合物样品的组成,称取四份质量均为2.96g的固体溶于水,分别往四份溶液中逐滴加入不同体积1.00mol·L-1的盐酸,加入盐酸溶液的体积和收集到CO2气体的体积(忽略气体在水中的溶解,气体体积均已折算成标准状况下的体积)如表所示:
实验序号 | 1 | 2 | 3 | 4 |
盐酸体积/mL | 20 | 40 | 60 | 80 |
CO2体积/mL | 0 | 448 | 672 | 672 |
下列说法不正确的是
A.实验1中发生反应的离子方程式为:CO![]() +H+=HCO
+H+=HCO![]()
B.实验2溶液中,含有NaCl、Na2CO3和NaHCO3三种溶质
C.实验3和实验4蒸干溶液所得固体一定是NaCl
D.原固体混合物中Na2CO3和NaHCO3的物质的量之比为2:1