题目内容
4.烷烃A只可能有三种一氯取代产物B、C和D.C的结构简式是(CH3)2C(CH2CH3)CH2Cl.B和D分别与强碱的醇溶液共热,都只能得到有机化合物E.各物质间关系如图所示.
(1)写出结构简式:A(CH3)3CCH2CH3; G(CH3)3CCH2CHO
(2)写出反应类型:B→F取代反应;B→E消去反应;
(3)写出D→E反应方程式:(CH3)3CCH(Cl)CH3+NaOH$→_{△}^{醇}$(CH3)3CCH=CH2+NaCl+H2O.
分析 烷烃A只可能有三种一氯取代产物B、C和D,C的结构简式是(CH3)2C(CH2CH3)CH2Cl,故A为(CH3)3CCH2CH3,B和D分别与强碱的醇溶液共热,发生消去反应,都只能得到有机化合物E,故E为(CH3)3CCH=CH2,B在氢氧化钠水溶液下发生水解(取代)反应生成F,F为醇,F氧化生成G,G能进一步发生银镜反应得H,G含有醛基-CHO,故B为(CH3)3CCH2CH2Cl,F为(CH3)3CCH2CH2OH,G为(CH3)3CCH2CHO,H为(CH3)3CCH2COOH,所以D为(CH3)3CCH2ClCH3,据此答题.
解答 解:烷烃A只可能有三种一氯取代产物B、C和D,C的结构简式是(CH3)2C(CH2CH3)CH2Cl,故A为(CH3)3CCH2CH3,B和D分别与强碱的醇溶液共热,发生消去反应,都只能得到有机化合物E,故E为(CH3)3CCH=CH2,B在氢氧化钠水溶液下发生水解(取代)反应生成F,F为醇,F氧化生成G,G能进一步发生银镜反应得H,G含有醛基-CHO,故B为(CH3)3CCH2CH2Cl,F为(CH3)3CCH2CH2OH,G为(CH3)3CCH2CHO,H为(CH3)3CCH2COOH,所以D为(CH3)3CCH2ClCH3,
(1)根据上面的分析可知,A为(CH3)3CCH2CH3,G为(CH3)3CCH2CHO,
故答案为:(CH3)3CCH2CH3;(CH3)3CCH2CHO;
(2)根据上面的分析可知,B→F为取代反应,B→E为消去反应,
故答案为:取代反应;消去反应;
(3)D→E反应方程式为(CH3)3CCH(Cl)CH3+NaOH$→_{△}^{醇}$(CH3)3CCH=CH2+NaCl+H2O,
故答案为:(CH3)3CCH(Cl)CH3+NaOH$→_{△}^{醇}$(CH3)3CCH=CH2+NaCl+H2O;
点评 本题考查有机物推断,注意根据A一氯代物的性质进行推断,需要学生熟练掌握官能团的性质与转化,难度中等.

| A. | 聚乙烯 | B. | 氯化钠 | C. | 淀粉 | D. | 聚1,3-丁二烯 |
 (1)T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示,根据图示可知:A与B反应生成C的化学方程式为A(g)+3B(g)?2C(g).
(1)T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示,根据图示可知:A与B反应生成C的化学方程式为A(g)+3B(g)?2C(g).(2)在80℃时,将0.40mol 的N2O4气体充入2L 已经抽空的固定容积的密闭容器中,发生如下反应:N2O4?2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间/s n/mol | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
| A. | 对二甲苯 | B. | 丙烯 | C. | 丙炔 | D. | 溴乙烷 |
| 化学键 | H-H | H-Cl | H-I | Cl-Cl | Br-Br |
| 键能/kJ/mol | 436 | 431 | 299 | 247 | 193 |
| A. | HCl | B. | HBr | C. | H2 | D. | Br2 |
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
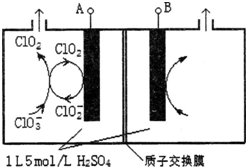 研究含Cl、N、S等元素的化合物对净化水质、防治污染有重要意义.
研究含Cl、N、S等元素的化合物对净化水质、防治污染有重要意义. 化合物A、B可合成荧光“魔棒”中产生能量的物质之一(CPPO).
化合物A、B可合成荧光“魔棒”中产生能量的物质之一(CPPO).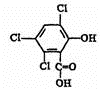 .
. .
.