题目内容
11.现有原子序数为1~20元素的元素性质或原子结构如下,按要求回答下列有关问题:(1)元素甲是第3周期ⅦA族元素,甲元素与另两种非金属元素可组成离子化合物A.写出A的化学式NH4Cl,A中含有的化学键是离子键、共价键.
(2)在第3周期元素的原子半径中(0族除外),元素乙的原子半径最大,写出元素乙的最高价氧化物对应水化物的电子式
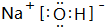 .
.(3)金属元素丙形成的某化合物的溶液常用于检验CO2,则元素丙的简单离子与元素甲的简单离子的半径大小关系是r(Cl-)>r(Ca2+)(用离子符号表示),元素丁的原子序数比丙小8,写出元素丁的单质在CO2中燃烧的化学方程式2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
(4)元素戊是第3周期中简单离子半径最小的元素,写出该元素的最高价氧化物对应水化物与乙元素的最高价氧化物对应水化物溶液反应的离子方程式:Al(OH)3+OH-═AlO2-+2H2O.
分析 (1)元素甲是第3周期ⅦA族元素,则甲为Cl,甲元素与另两种非金属元素可组成离子化合物A,应是铵盐,即A为氯化铵,含有离子键与共价键;
(2)在第3周期元素的原子半径中(0族除外),元素乙的原子半径最大,则乙为Na,其最高价氧化物对应水化物为NaOH,由钠离子与氢氧根离子构成;
(3)金属元素丙形成的某化合物的溶液常用于检验CO2,则丙为Ca,电子层结构相同的离子,核电荷数越大离子半径越小;
元素丁的原子序数比丙小8,则丁为Mg,Mg在CO2中燃烧生成MgO与碳;
(4)元素戊是第3周期中简单离子半径最小的元素,则戊为Al,该元素的最高价氧化物对应水化物为氢氧化铝,与氢氧化钠反应生成偏铝酸钠与水.
解答 解:(1)元素甲是第3周期ⅦA族元素,则甲为Cl,甲元素与另两种非金属元素可组成离子化合物A,应是铵盐,即A为NH4Cl,含有离子键与共价键,故答案为:NH4Cl;离子键、共价键;
(2)在第3周期元素的原子半径中(0族除外),元素乙的原子半径最大,则乙为Na,其最高价氧化物对应水化物为NaOH,由钠离子与氢氧根离子构成,电子式为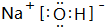 ,
,
故答案为: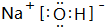 ;
;
(3)金属元素丙形成的某化合物的溶液常用于检验CO2,则丙为Ca,电子层结构相同的离子,核电荷数越大离子半径越小,故离子半径:r(Cl-)>r(Ca2+);
元素丁的原子序数比丙小8,则丁为Mg,Mg在CO2中燃烧生成MgO与碳,反应方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,
故答案为:r(Cl-)>r(Ca2+);2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;
(4)元素戊是第3周期中简单离子半径最小的元素,则戊为Al,该元素的最高价氧化物对应水化物为氢氧化铝,与氢氧化钠反应生成偏铝酸钠与水,反应离子方程式为:Al(OH)3+OH-═AlO2-+2H2O,
故答案为:Al(OH)3+OH-═AlO2-+2H2O.
点评 本题考查了位置、结构与性质关系的综合应用,题目难度中等,明确元素周期律内容、元素周期表结构为解答关键,试题知识点较多、综合性较强,充分开心学生的分析、理解能力及灵活应用能力.

 学习实践园地系列答案
学习实践园地系列答案| A. | 将钠放入水中,钠将沉在水底 | |
| B. | 将一小块钠放在稀盐酸中,钠将与水反应生成NaOH和H2,生成的NaOH再与HCl反应生成NaCl和H2O | |
| C. | 将一小块钠放在CuSO4溶液中发生如下反应:2Na+CuSO4═Na2SO4+Cu | |
| D. | Na2O和Na2O2中,氧元素化合价不同 |
| 固体成分 | 气体成分 | |
| A | Na2CO3 | CO2、H2O、O2 |
| B | Na2CO3 | H2O、O2 |
| C | Na2CO3、Na2O2 | O2 |
| D | Na2CO3、Na2O2、NaOH | O2 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 1molCl2与足量的铁反应生成FeCl3,转移的电子数是3NA | |
| B. | 1mol氧气含有的原子数是1mol氖气含有的原子数的两倍 | |
| C. | 7.8g Na2O2中含有阴离子的数目为0.1NA,与足量水反应时电子转移了0.1NA | |
| D. | 在标准状况下,NA个水分子所占有的体积约为22.4L |
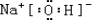 ;w属于非极性 (填“极性”或“非极性)分子;
;w属于非极性 (填“极性”或“非极性)分子;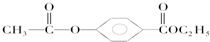 .A经①②两步反应得到C、D和E.B经①②两步反应得E、F和H.上述反应过程、产物性质及相互关系如图所示.
.A经①②两步反应得到C、D和E.B经①②两步反应得E、F和H.上述反应过程、产物性质及相互关系如图所示.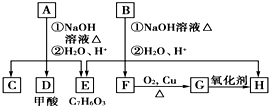
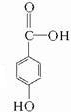 .
.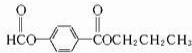 和
和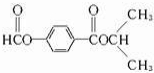 .
. 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.图2是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.完成下列填空:
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.图2是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.完成下列填空: