题目内容
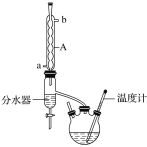
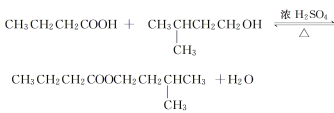
【题目】丁酸异戊酯又称香蕉油,多用于食品和化妆品的香精,实验室用正丁酸与异戊醇反应制备丁酸异戊酯,有关数据和装置示意图如下:
相对分子质量 | 密度(g·cm-3) | 沸点(℃) | 水中溶解性 | |
正丁酸 | 88 | 0.958 7 | 163.5 | 溶 |
异戊醇 | 88 | 0.813 2 | 131 | 微溶 |
丁酸异戊酯 | 158 | 0.886 | 179 | 不溶 |
实验步骤:
①如图连接好装置,在三颈烧瓶中加入0.2 mol异戊醇、0.1 mol正丁酸、数滴浓硫酸、5 mL苯和2~3片碎瓷片。充分摇匀,分水器内加入异戊醇直至与支管相平;
②在122~132℃下回流反应1.5h即可得粗产品;
③冷却后用10%的NaOH溶液中和用水洗至中性,加入无水硫酸镁后蒸馏得较纯净的丁酸异戊酯11g。
回答下列问题:
(1)图中A仪器的名称是___________。
(2)在该实验中,三颈烧瓶的容积最适合的是_____(填字母)。
A.50mL B.100mL C.200mL
(3)加入碎瓷片的作用是______;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是_____(填字母)。
A.冷却后补加 B.立即补加 C.不需补加 D.重新配料
(4)分离提纯过程中加入无水硫酸镁的目的是______________。
(5)在蒸馏得较纯净的丁酸异戊酯操作中,仪器选择及安装都正确的是_______(填字母)。

(6)本实验的产率是______(保留三位有效数字)。
【答案】球形冷凝管或冷凝管 B 防止暴沸 A 干燥 b 69.6%
【解析】
(1)根据仪器A的构造写出其名称;
(2)根据反应物的物质的量计算出质量,再计算出需要各物质的体积,根据计算出的总体积判断需要三颈烧瓶的最佳容积;
(3)碎瓷片可以防止混合液在加热时发生暴沸现象;如果加热一段时间后发现忘记加碎瓷片,应冷却至室温,补加碎瓷片;
(4)无水MgSO4的具有吸水性;
(5)根据温度计在蒸馏操作中的作用结合冷凝管的作用分析判断;
(6)根据产率=![]() ×100%进行计算。
×100%进行计算。
(1)根据A的构造可知,仪器A为球形冷凝管或冷凝管,故答案为:球形冷凝管或冷凝管;
(2)0.2mol异戊醇的体积约为![]() ≈21.6mL,0.1mol正丁酸的体积约为
≈21.6mL,0.1mol正丁酸的体积约为![]() ≈9.2mL,还有5mL苯,混合液总体积大于21.6mL+9.2mL+5mL=35.8mL,三颈烧瓶的容积应该为溶液体积的2倍左右,所以三颈烧瓶的最佳容积为100mL,所以B正确,故答案为:B;
≈9.2mL,还有5mL苯,混合液总体积大于21.6mL+9.2mL+5mL=35.8mL,三颈烧瓶的容积应该为溶液体积的2倍左右,所以三颈烧瓶的最佳容积为100mL,所以B正确,故答案为:B;
(3)混合液体加热时容易发生暴沸现象,所以加入碎瓷片可防止液体暴沸;液体加热要加碎瓷片,防止暴沸,如果加热一段时间后发现忘记加碎瓷片,应冷却至室温,补加碎瓷片,所以A正确,故答案为:防止暴沸;A;
(4)酯化反应是可逆反应,增加一种反应物的物质的量可以提高另一种反应物的转化率,所以加入过量异戊醇可以提高正丁酸的转化率;无水MgSO4的具有吸水性,所以分离提纯过程中加入无水硫酸镁可以干燥丁酸异戊酯,故答案为:干燥;
(5)在蒸馏操作中,温度计的水银球要放在蒸馏烧瓶的支管口处,所以ad错误,用冷凝水冷却时一般需要直型冷凝管,而不选用球形冷凝管,所以仪器及装置安装正确的是b,故答案为:b;
(6)0.2mol异戊醇和0.1mol正丁酸反应,理论上可以生成0.1mol丁酸异戊酯,质量为:158g/mol×0.1mol=15.8g,而实际产量是11g,所以本次实验的产率=![]() ×100%=69.6%,故答案为:69.6%。
×100%=69.6%,故答案为:69.6%。

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向KI溶液中滴入少量新制氯水和四氯化碳,振荡、静置,溶液下层呈紫红色 | I的还原性强于Cl |
B | 向无水乙醇中加入浓H2SO4,加热,将产生的气体通入酸性KMnO4溶液,紫红色褪去 | 该气体一定是乙烯 |
C | 测定Na2CO3和Na2SiO3溶液的pH,后者pH比前者的大 | C的非金属性比Si强 |
D | 向1-溴丙烷中加入KOH溶液,加热几分钟,冷却后再加入AgNO3溶液,无淡黄色沉淀生成 | 1-溴丙烷没有水解 |
A.AB.BC.CD.D