题目内容
【题目】下列说法正确的是
A. 键角:BF3>CH4>H2O>NH3
B. CO2、HClO、HCHO分子中一定既有σ键又有π 键
C. 已知二茂铁(Fe(C5H5)2)熔点是173 ℃(在100 ℃时开始升华),沸点是249℃,不溶于水,易溶于苯等非极性溶剂。在二茂铁结构中,C5H5 -与Fe2+之间是以离子键相结合
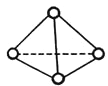
D. 在硅酸盐中,SiO44-四面体通过共用顶角氧离子形成一种无限长单链结构的多硅酸根如图a,其中Si原子的杂化方式与b图中S8单质中S原子的杂化方式相同

【答案】D
【解析】
A. BF3:立体形状平面三角形,键角120![]() ;CH4:立体形状正四面体形,键角109
;CH4:立体形状正四面体形,键角109![]() 28′;H2O:立体呈角形(V),形键角105
28′;H2O:立体呈角形(V),形键角105![]() ;NH3:立体形状三角锥形,键角107
;NH3:立体形状三角锥形,键角107![]() ,所以键角:BF3>CH4>NH3>H2O,故A错误;
,所以键角:BF3>CH4>NH3>H2O,故A错误;
B. CO2既有σ键又有π键;H-O-Cl 只有σ键;H-CHO既有σ键又有π键;故B错误;
C. 在二茂铁结构中,不存在C5H5 -与Fe2+,碳原子含有孤对电子,铁含有空轨道,所以碳原子和铁原子之间形成配位键,故C错误;
D. 硅酸盐中的硅酸根(SiO44 )为正四面体结构,所以中心原子Si原子采取了sp3杂化方式;S8单质中S原子有两个孤对电子和两个共价键,杂化方式也为sp3,故D正确。
所以D选项是正确的。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目