题目内容
下列物质中,只含有离子键的化合物是( )
| A、KOH |
| B、NH4Cl |
| C、HCl |
| D、MgCl2 |
考点:离子化合物的结构特征与性质
专题:化学键与晶体结构
分析:一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,据此分析解答.
解答:
解:A.KOH中钾离子和氢氧根离子之间存在离子键、O原子和H原子之间存在共价键,故A错误;
B.氯化铵中铵根离子和氯离子之间存在离子键、N原子和H原子之间存在共价键,故B错误;
C.HCl分子中H原子和Cl原子之间只存在共价键,为共价化合物,故C错误;
D.氯化镁中镁离子和氯离子之间只存在离子键,故D正确;
故选D.
B.氯化铵中铵根离子和氯离子之间存在离子键、N原子和H原子之间存在共价键,故B错误;
C.HCl分子中H原子和Cl原子之间只存在共价键,为共价化合物,故C错误;
D.氯化镁中镁离子和氯离子之间只存在离子键,故D正确;
故选D.
点评:本题考查了离子键和共价键的判断,明确离子键和共价键的区别是解本题关键,注意氯化镁中两个氯离子之间不存在化学键,为易错点.

练习册系列答案
相关题目
对于主族元素R形成化合物的分子式为HROm,其水溶液呈酸性,下列说法中正确的是( )
| A、m越大,其HROm的氧化性越强 |
| B、m越大,其HROm的酸性越强 |
| C、与Zn反应时,只能产生一种气体 |
| D、当m=3时,R一定为ⅤA族 |
下列有关反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H(298K)=-905kJ?mol-1的描述正确的是( )
| A、生成物的总能量大于反应物的总能量 |
| B、该反应为放热反应 |
| C、该反应中每4 mol NH3(g)被氧化,吸收905 kJ热量 |
| D、该反应为吸热反应 |
某无色溶液中能大量共存的一组离子是( )
| A、OH-、Ba2+、NH4+、Cl- |
| B、K+、Fe2+、H+、NO3- |
| C、NH4+、Al3+、Cl-、NO3- |
| D、Mg2+、SO42-、SiO32-、H+ |
下列有关物质应用的说法错误的是( )
| A、CCl4曾用作灭火剂,但因与水在高温下反应会产生有毒物质,现已被禁用 |
| B、工厂中常用的静电除尘装置是根据胶体带电这个性质而设计的 |
| C、Li是最轻的金属,也是活动性较强的金属,是制造电池的理想物质 |
| D、为了延长果实或花朵的成熟期,可用浸泡过高锰酸钾溶液的硅土吸收水果或花朵产生的乙烯 |
把铁片加到1L 1mol/L的氯化铁溶液中,当反应后溶液中Fe3+和Fe2+物质的量浓度相等时,铁片减少的质量为( )
| A、2.8g | B、5.6g |
| C、11.2g | D、1.4g |
下列物质在一定条件下彻底水解,其产物不只一种的是( )
| A、淀粉 | B、纤维素 |
| C、蔗糖 | D、麦芽糖 |
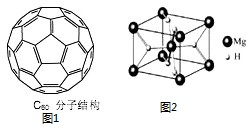 氢的存储是氢能应用的主要瓶颈,目前所采用或正在研究的主要储氢材料有:配位氢化物、富氢载体化合物、碳质材料、金属氢化物等.
氢的存储是氢能应用的主要瓶颈,目前所采用或正在研究的主要储氢材料有:配位氢化物、富氢载体化合物、碳质材料、金属氢化物等.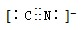
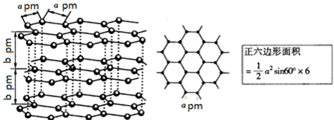 2012年宾夕法尼亚大学研究人员展示了一种硒化镉纳米晶体,它能被“印”或“涂”在柔软塑料上,制成多种性能优良的电子设备.请回答下列问题:
2012年宾夕法尼亚大学研究人员展示了一种硒化镉纳米晶体,它能被“印”或“涂”在柔软塑料上,制成多种性能优良的电子设备.请回答下列问题: