题目内容
把铁片加到1L 1mol/L的氯化铁溶液中,当反应后溶液中Fe3+和Fe2+物质的量浓度相等时,铁片减少的质量为( )
| A、2.8g | B、5.6g |
| C、11.2g | D、1.4g |
考点:化学方程式的有关计算
专题:计算题
分析:铁粉放入三氯化铁溶液中发生反应Fe+2Fe3+=3Fe2+,已反应的Fe3+的物质的量为1mol,根据方程式计算生成的Fe2+的物质的量,进而得到未反应的Fe3+的物质的量,二者之比即为答案.
解答:
解:设参加反应的铁为xmol,则:
Fe+2Fe3+=3Fe2+
xmol 2xmol 3xmol
溶液中的Fe3+和Fe2+浓度相等,即1-2x=3x,所以x=0.2mol,
反应的铁的质量为:0.2mol×56g/mol=11.2g,
故选C.
Fe+2Fe3+=3Fe2+
xmol 2xmol 3xmol
溶液中的Fe3+和Fe2+浓度相等,即1-2x=3x,所以x=0.2mol,
反应的铁的质量为:0.2mol×56g/mol=11.2g,
故选C.
点评:本题考查氧化还原反应,侧重于学生的分析能力和计算能力的考查,为高频考点,注意结合反应的离子方程式计算该题,难度不大.

练习册系列答案
相关题目
下列物质中,只含有离子键的化合物是( )
| A、KOH |
| B、NH4Cl |
| C、HCl |
| D、MgCl2 |
若锌与稀硝酸反应时,其化学反应方程式为4Zn+10HNO3═aZn(NO3)2+bM+cH2O,则a、b、c、M可能分别为( )
| A、4、1、5、N2O |
| B、4、2、4、NO2 |
| C、4、1、3、N2O4 |
| D、4、3、5、NO |
下列反应的离子方程式不正确的是( )
| A、碳酸氢钙溶液加入过量的氢氧化钙溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O |
| B、等物质的量的NH4HCO3与NaOH在溶液中反应:NH4++OH-═NH3?H2O |
| C、在含有Mn2+的溶液中加入HNO3酸化,再加入PbO2,反应体系显紫红色5PbO2+2Mn2++4H+═5Pb2++2MnO4-+2H2O |
| D、等体积同浓度NaHSO4、Ba(OH)2两溶液混合:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
下列说法正确的是( )
| A、用钠可以检验乙醇中是否含有水 |
| B、1mol二甘醇(HO-CH2CH2OCH2CH2-OH)和足量的钠反应可以产生0.5mol H2 |
| C、乙醇和乙酸在浓硫酸加热条件下的反应是取代反应 |
| D、葡萄糖和新制Cu(OH)2悬浊液加热沸腾生成砖红色沉淀反应是加成反应 |
下列物质既能发生消去反应,又能氧化成醛的是( )
| A、苯甲醇 |
| B、2,2-二甲基-1-丙醇 |
| C、2-甲基-1-丁醇 |
| D、甲醇 |
从原料和环境方面的要求看,绿色化学对生产中的化学反应提出一个提高原子利用率的要求,即尽可能不采用那些对产品的化学组成来说没有必要的原料.现有下列3种合成苯酚的反应路线:
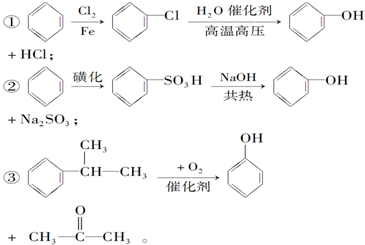
其中符合原子节约要求的生产过程是( )

其中符合原子节约要求的生产过程是( )
| A、③ | B、② | C、① | D、①②③ |
下列说法正确的是( )
A、按系统命名法,化合物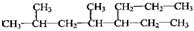 的名称为2,4-二甲基-5-丙基庚烷 的名称为2,4-二甲基-5-丙基庚烷 |
| B、人们生活中经常接触的聚乙烯、聚氯乙烯、聚苯乙烯、ABS工程塑料、顺丁橡胶等制品都是通过加聚反应得到的 |
| C、若两种二肽互为同分异构体,则二者的水解产物一定不相同 |
| D、分子式为C4H8Br2的有机物,结构中只含一个甲基的同分异构体(不考虑立体异构)有5种 |